Fisiopatología molecular de la inflamación y fibrosis peritoneal (PERINFIB)
Resumen de Investigación:
Utilizada para tratar la enfermedad renal crónica avanzada, la diálisis peritoneal (DP) consiste en utilizar el peritoneo como una membrana semipermeable a través de la cual se realiza la difusión y la ultrafiltración. Durante la DP, el peritoneo se expone a soluciones bio-incompatibles que causan inflamación, angiogénesis y fibrosis, lo que resulta en un fallo de la membrana. Nuestro grupo ha demostrado que las células mesoteliales experimentan una transición epitelial-mesenquimal (EMT) en respuesta al daño peritoneal (Figura 1). Durante los últimos 16 años, numerosas publicaciones apuntan a que la EMT mesotelial (también denominada Transición Mesotelial a Mesenquimal, MMT) es un buen marcador para el fallo de la membrana y una diana terapéutica para prevenir la fibrosis y / o angiogénesis inducida por la DP.
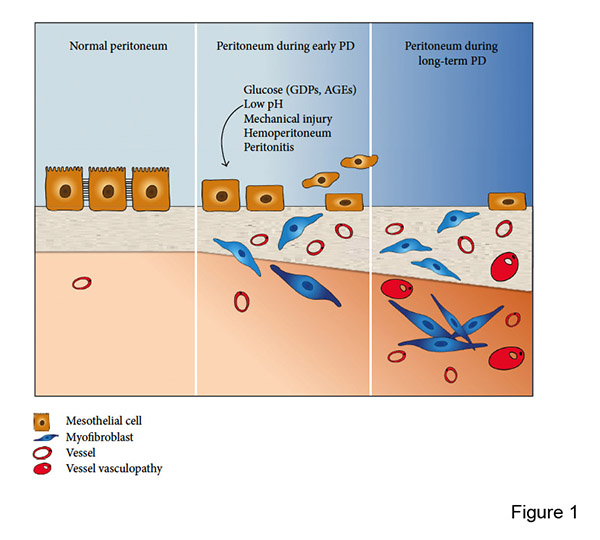
Figura 1. En el peritoneo se generan nuevas células fibroblásticas a través de la conversión local de las células mesoteliales (MCs), por transición epitelio mesénquima (TEM), durante la diálisis peritoneal. Las MCs transdiferenciadas invaden el estroma submesotelial y allí participan en los procesos de fibrosis y angiogénesis, que posteriormente darán lugar al fallo de ultrafiltración peritoneal.
Recientemente, nos planteamos si la EMT desempeña un papel en otras patologías peritoneales como la metástasis peritoneal y las adherencias posquirúrgicas. La metástasis peritoneal es una complicación de los carcinomas abdominales (por ejemplo, carcinoma de ovario) para la cual no existe una terapia efectiva. La progresión de los implantes metastásicos se ve afectada por los fibroblastos asociados al carcinoma (CAF), que pueden derivar de varios tipos de células. Nosotros hemos demostrado en biopsias de implantes peritoneales humanos que una subpoblación de CAF deriva de las células mesoteliales a través de EMT. Nuestros resultados también sugieren que esta EMT hace que el peritoneo sea más receptivo a la implantación de células tumorales, contribuye al crecimiento y la vascularización de los tumores secundarios y que la EMT es una diana terapéutica en la carcinomatosis peritoneal (Figura 2).
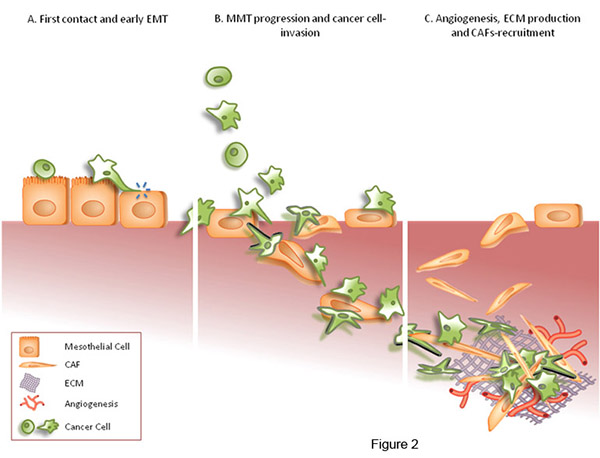
Figura 2. La diseminación peritoneal es una ruta frecuente de metástasis para los cánceres de ovario y del tracto gastrointestinal. Nosotros hemos demostrado que en los implantes metastáticos peritoneales una subpoblación de fibroblastos asociados a carcinoma (CAFS) derivan de las células mesoteliales vía transición mesotelio mesénquima (MMT). Ademas, la MMT promueve la adhesión e invasión de las células tumorales.
Las adherencias son áreas de tejido fibrótico que unen tejidos y órganos que normalmente no estarían conectados y que pueden poner en peligro la vida. La mayoría de las adherencias son posquirúrgicas. El análisis histológico de las adherencias postquirúrgicas humanas ha demostrado que las células mesoteliales adyacentes al tejido fibrótico muestran signos de EMT, lo que sugiere que esto podría ser un paso inicial en su desarrollo. Los procesos fisiopatológicos involucrados en su formación siguen siendo desconocidos. Nuestros resultados recientes han demostrado que el daño mecánico es el principal inductor de EMT durante la formación de adherencias. En consecuencia, las moléculas involucradas en la mecano-transducción, como la caveolina 1 (CAV-1), podrían desempeñar un papel en la modulación de la EMT mecánica y la formación de adherencias (Figura 3).
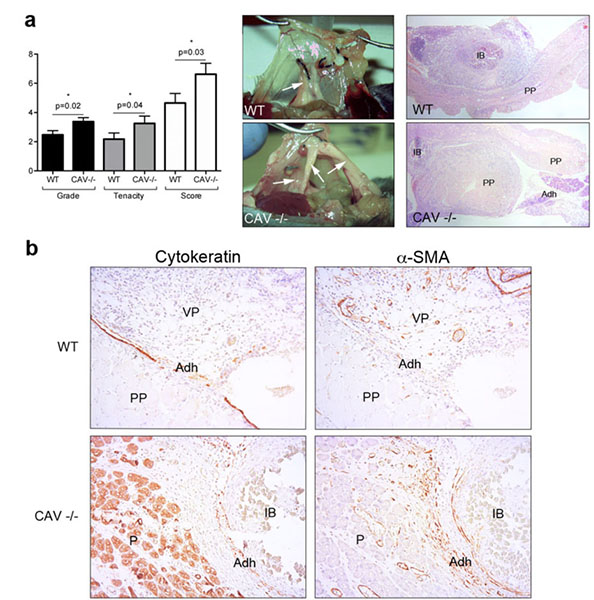
Figura 3. a) Los experimentos de adhesión peritoneal, basados en botones isquémicos, mostraron que los ratones Cav-1 KO tienen mayor capacidad para desarrollar adherencias en comparación con los ratones WT. b) El análisis inmunohistoquímico, en secciones en serie de biopsias peritoneales, mostró que los ratones Cav-1 KO tienen signos exacerbados de transición mesotelial a mesenquimal, como lo demuestra la coexpresión de citoqueratina y α-SMA en células fibroblásticas estromales.
El objetivo de nuestro trabajo es ampliar el conocimiento de las implicaciones patológicas de la EMT de las células mesoteliales y los mecanismos moleculares que regulan este proceso, e identificar dianas moleculares para el diseño de estrategias terapéuticas, con posibles aplicaciones en enfermedades asociadas con la fibrosis peritoneal/ angiogénesis y en metástasis peritoneales.

| Apellidos | Nombre | Laboratorio | Ext.* | Categoría profesional | |
|---|---|---|---|---|---|
| López Cabrera | Manuel | 406 | 4604/4707 | mlcabrera(at)cbm.csic.es | E. Profesores de Investigación de Organismos Públicos de Investigación |
| Sandoval Correa | Mª Pilar | 406 | 4707 | psandoval(at)cbm.csic.es | M3 |
| Tomero Sanz | Henar | 406 | 4707 | htomero(at)cbm.csic.es | Titulado Sup. Actividades Tecn. y Prof.GP1 |
Publicaciones relevantes:
-
Strippoli R, Sandoval P, Moreno-Vicente R, Rossi L, Battistelli C, Terri M, Pascual-Antón L, Loureiro M, Matteini F, Calvo E, Jiménez-Heffernan JA, Gómez MJ, Jiménez-Jiménez V, Sánchez-Cabo F, Vázquez J, Tripodi M, López-Cabrera M, Del Pozo MÁ. Caveolin1 and YAP drive mechanically induced mesothelial to mesenchymal transition and fibrosis.Cell Death Dis. 2020 Aug 3;11(8):647. doi: 10.1038/s41419-020-02822-1.
-
Gordillo CH, Sandoval P, Muñoz-Hernández P, Pascual-Antón L, López-Cabrera M, Jiménez-Heffernan JA. Mesothelial-to-Mesenchymal Transition Contributes to the Generation of Carcinoma-Associated Fibroblasts in Locally Advanced Primary Colorectal Carcinomas. Cancers (Basel). 2020 Feb 21;12(2):499. doi: 10.3390/cancers12020499.
-
Raby AC, González-Mateo GT, Williams A, Topley N, Fraser D, López-Cabrera M, Labéta MO. Targeting Toll-like receptors with soluble Toll-like receptor 2 prevents peritoneal dialysis solution-induced fibrosis. Kidney Int. 2018 Aug;94(2): 346-362
- Horejs CM, St-Pierre JP, Ojala JRM, Steele JAM, da Silva PB, Rynne-Vidal A, Maynard SA, Hansel CS, Rodríguez-Fernández C, Mazo MM, You AYF, Wang AJ, von Erlach T, Tryggvason K, López-Cabrera M, Stevens MM. Preventing tissue fibrosis by local biomaterials-interfacing of specific cryptic extracellular matrix information. Nat Commun. 2017 Jun 8;8:15509.
- Rynne-Vidal A, Au-Yeung CL, Jiménez-Heffernan JA, Pérez-Lozano ML, Cremades-Jimeno L, Bárcena C, Cristóbal-García I, Fernández-Chacón C, Yeung TL, Mok SC, Sandoval P, López-Cabrera M. Mesothelial-to-mesenchymal transition as a possible therapeutic target in peritoneal metastasis of ovarian cancer J Pathol. 2017 Jun;242(2):140-151.
- Liappas G, González-Mateo GT, Sánchez-Díaz R, Lasarte S, Matesanz-Marín A, Zur R, Ferrantelli E, García Ramírez L Aguilera A, Fernández-Ruiz E, Beelen RHJ, Selgas R, Sánchez-Madrid F, Martín P, López-Cabrera M. Immune-regulatory molecule CD69 controls peritoneal fibrosis. J Am Soc Nephrol. 2016 Dec;27(12):3561-3576.
- Sandoval P, Jiménez-Heffernan JA, Guerra-Azcona G, Pérez-Lozano ML, Rynne-Vidal A, Martín P, Coronado MJ, Dotor J, Aguilera A, López-Cabrera M. Mesothelial-to-mesenchymal transition in the pathogenesis of post-surgical peritoneal adhesions. J Pathology 2016 May;239(1): 48-59. doi: 10.1002/path.4695.
- Strippoli R, Loureiro J, Moreno V, Benedicto I, Pérez Lozano ML, Barreiro O, Pellinen T, Minguet S, Foronda M, Osteso MT, Calvo E, Vázquez J, López-Cabrera M, Del Pozo MA. Caveolin-1 deficiency induces a MEK-ERK1/2-Snail-1-dependent epithelial-mesenchymal transition and fibrosis during peritoneal dialysis. EMBO Mol Med. 2014 Dec 30;7(1): 102-23.
- Sandoval P, Jiménez-Heffernan JA, Rynne-Vidal A, Pérez-Lozano ML, Gilsanz A, Ruiz-Carpio V, Reyes R, García-Bordas J, Stamatakis K, Dotor J, Majano PL, Fresno M, Cabañas C, López-Cabrera M. Carcinoma-associated fibroblasts derive from mesothelial cells via mesothelial to mesenchymal transition in peritoneal metastasis. J Pathology. 2013 Dec;231(4): 517-531.
- Loureiro J, Aguilera A, Selgas R, Sandoval P, Albar-Vizcaíno P, Pérez-Lozano ML, Ruíz-Carpio V, Majano PL, Lamas S, Rodríguez-Pascual F, Borras-Cuesta F, Dotor J, López Cabrera M. Blocking TGF-β1 Protects the Peritoneal Membrane from Dialysate-Induced Damage. J Am Soc Nephrol. 2011 Sep;22(9): 1682-1695.
- Aroeira LS, Lara-Pezzi E, Loureiro J, Aguilera A, Ramírez-Huesca M, González-Mateo G, Pérez-Lozano ML, Albar-Vizcaíno P, Bajo MA, del Peso G, Sánchez-Tomero JA, Jiménez-Heffernan JA, Selgas R and López-Cabrera M. Cyclooxygenase-2 Mediates Dialysate Induced Alterations of the Peritoneal Membrane. J Am Soc Nephrol. 2009 Mar;20(3): 582-592.
- Yáñez-Mó M, Lara-Pezzi E, Selgas R, Ramírez-Huesca M, Domínguez-Jiménez C, Jiménez-Heffernan JA, Aguilera A, Sánchez-Tomero JA, Bajo MA, Alvarez V, Castro MA, del Peso G, Cirujeda A, Gamallo C, Sánchez-Madrid F, and López-Cabrera M. Peritoneal dialysis and epithelial-mesenchymal transition of mesothelial cells. N Engl J Med. 2003 Jan 30;348(5): 403-413.
Tesis doctorales:
- Angela Rynne-Vidal (2016). El origen mesotelial de los fibroblastos asociados a cáncer en la metástasis peritoneal. La transición mesotelio-mesénquima como posible diana terapéutica. Universidad Autónoma de Madrid.
- Vicente Ruiz Carpio (2015). Análisis de la huella genética de la transición mesotelio mesenquimal: Caracterización de nuevos marcadores en dialysis peritoneal. Universidad Complutense de Madrid
- Georgios Liappas (2015). Early leukocyte activation receptor CD69: a novel player in the maintenance of the TH17/Treg balance peritoneal fibrosis. Universidad Autónoma de Madrid.
- María Luisa Pérez Lozano (2013). Transición epitelio-mesenquimal inducida durante la diálisis peritoneal: efecto de los líquidos biocompatibles e importancia funcional de VEGF y sus receptores. Universidad Autónoma de Madrid.
- Guadalupe Tirma González Mateo (2011). Caracterización y modulación de la inflamación peritoneal para limitar la fibrosis causada por el líquido de diálisis: modelo de ratón. Universidad Complutense de Madrid. Director: Manuel López Cabrera y Rafael Selgas Gutiérrez.
- Ignacio Benedicto Español (2011). Interrelación entre proteínas asociadas a uniones intercelulares estrechas, polaridad de los hepatocitos y el virus de la hepatitis C. Universidad Autónoma de Madrid. Directores: Manuel López Cabrera y Pedro Lorenzo Majano Rodríguez.
- Jesús Loureiro Álvarez (2011). Transición epitelio-mesenquimal como diana terapéutica en modelos experimentales de diálisis peritoneal. Universidad Autónoma de Madrid. Director: Manuel López Cabrera.
Patentes:
- Inventors: Manuel López-Cabrera, Abelardo Aguilera, Rafael Selgas, Jutta Passlick-Deetjen, Janine Buechel, Sonja Steppan. Title: Method and kit for diagnosing epithelial to mesenchymal transition of the peritoneum. German Patent Number: DE 102015115158.8. (Granted). Date of Priority: 09/09/2015. Date of granting: 13/07/2017. International applications: PCT/EP2016/071149 WO2017042253 (A1). Extended Countries: USA patent: US 2018/0246098 A1, China patent: CN108449998 (A)-2018-08-24
- Inventors: Abelardo Aguilera, Manuel López-Cabrera, Rafael Selgas, Jutta Passlick-Deetjen, Janine Büchel, Sonja Stephan. Title: Pharmaceutical Compositions Containing Steviosides. Application Number: Priority application EP 14 191 301.2. Date of Priority: October 31st, 2014. International applications: PCT/EP2015/074955 WO2016066672 (A1). Extended Countries: USA patent: US 2017/0304335 A1
Participación en proyectos financiados por la Unión Europea:
- TÍTULO DEL PROYECTO: Identification and Management of Patients at Risk – Outcome and Vascular Events in Peritoneal Dialysis (Acrómimo: IMPROVE-PD).
- TIPO DE CONTRATO: H2020-MSCA-ITN-2018 (Marie S-Curie Innovative Training Networks) (Grant # 812699)
- ADMINISTRACIÓN FINANCIADORA: EUROPEAN UNION
- ENTIDADES PARTICIPANTES: 11 grupos de investigación procedentes de siete países europeos.
- DURACIÓN, DESDE: 2018 HASTA: 2022
- INVESTIGADOR COORDINADOR: Manuel López Cabrera (CSIC)
- Total Financiación: 4.021.380 Euros.




















