Mecanismos inmunoreguladores en el desarrollo de la patogenia en la enfermedad de Chagas: aplicaciones traslacionales
Resumen de Investigación:
La enfermedad de Chagas causada por Trypanosoma cruzi afecta aproximadamente a 10 millones de personas en América Latina. Además, la transfusión de sangre y el trasplante de órganos es un problema sanitario en los países receptores de migrantes de zonas endémicas. La patología cardíaca es la manifestación más grave y característica y se estima una incidencia futura de entre 6.000 y 30.000 casos de miocardiopatía chagásica en España. Nuestra hipótesis de trabajo es que el desarrollo de la patología depende de una combinación de factores: antecedentes genéticos del huésped, diferentes capacidades de infectar parásitos con diferentes fondos genéticos y la respuesta inmune reguladora que afectarán al proceso inflamatorio e infeccioso. Las células mieloides supresoras (MDSC) se expanden durante la infección con cepas virulentas del parásito. La Figura 1 resume los mecanismos supresores generales de MDSC en contacto con células T. Por un lado, las MDSC expresan iNOS y NADPH oxidasa 2 (NOX-2) que producen especies reactivas de nitrógeno (RNS) y especies reactivas de oxígeno (ROS), respectivamente. La nitración y nitrosilación de proteínas por RNS conduce a la apoptosis y la inhibición de la fosforilación de proteínas y la degradación del ARNm de IL-2. Arginasa 1 (Arg1) e iNOS consumen L-arginina extracelular inhibiendo la expresión de la cadena ζ de CD3 e interfiriendo con la señalización de TCR. Arg1 produce L-ornitina que es el sustrato de poliaminas ligadas a la proliferación y colágeno involucrado en la reparación de tejidos y fibrosis. La ciclooxigenasa 2 (COX-2) y la prostaglandina E2 sintasa microsomal (mPGES-1) producen prostaglandina E2 supresora (PGE2). La indolamina 2,3-dioxigenasa (IDO) convierte el L-triptófano en L-quinurenina, que también bloquea la proliferación de células T. Por otro lado, el receptor SLAMF1 que interactúa con T. cruzi, puede desencadenar a través del adaptador EAT2 la conversión de PI en PI3P activando la NOX-2. Hemos observado que la infección por el parásito provoca la reducción de los niveles de L-arginina, que inhibe la proliferación de células T y RNS, incluido el óxido nítrico (NO) producido por la iNOS. La suplementación con L-arginina en ratones infectados produjo una disminución de la mortalidad y una mejora en el score clínico de los ratones, y podría usarse en una terapia combinada. Además, el receptor inmune SLAMF1, regulador de la producción de especies reactivas de oxígeno (ROS), inhibe la producción de ROS de manera dependiente de la cepa de parásito, por lo que la inhibición de la interacción de SLAMF1 con éste podría ser la base de una nueva terapia. Nuestro interés por la aplicación traslacional de nuestra investigación nos conduce a mantener colaboraciones científicas con grupos españoles y extranjeros, básicos y clínicos, para la evaluación de nuevos biomarcadores de pronóstico y seguimiento, necesarios para decidir el tratamiento de los pacientes y su eficacia. Para ello utilizamos herramientas “Ómicas” como Genómica, Transcriptómica, Proteómica y Metabolómica.
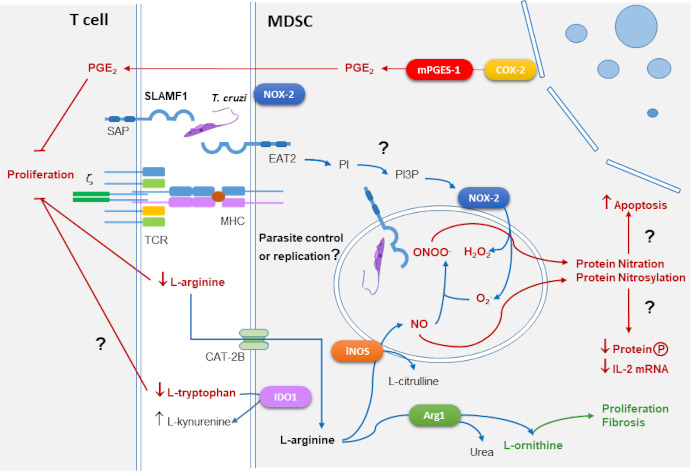
Figura 1. Principales mecanismos de la inmunosupresión de las células T mediada por las MDSC. Los signos de interrogación indican aquellos procesos que necesitan ser explorados más a fondo. (De Fresno M, Gironès N. 2021. Front Cell Infect Microbiol. Aug 27;11:737364).

| Apellidos | Nombre | Laboratorio | Ext.* | Categoría profesional | |
|---|---|---|---|---|---|
| Gironés Pujol | Nuria | 226 | 4593/4735 | ngirones(at)cbm.csic.es | Profesor Titular Universidad, GA |
| Santos Peñaloza | Diana Karolina | 226 | 4735 | Tco. de Investigación y Laboratorio | |
| Silva Padilla | Gissel Tamara | 226 | 4735 | Estudiante TFM |
Publicaciones relevantes:
- Fresno M, Gironès N (AC) (2/2). 2021. Myeloid-Derived Suppressor Cells in Trypanosoma cruzi Front Cell Infect Microbiol. Aug 27;11:737364.
- Callejas-Hernández F, Herreros-Cabello A, Del Moral-Salmoral J, Fresno M (AC), Gironès N (AC) (5/5). The Complete Mitochondrial DNA of Trypanosoma cruzi: Maxicircles and Minicircles. Front Cell Infect Microbiol. Jun 29;11:672448.
- Herreros-Cabello A, Callejas-Hernández F, Gironès N, Fresno M (3/4). Trypanosoma cruziGenome: Organization, Multi-Gene Families, Transcription, and Biological Implications. Genes (Basel). Oct 14;11(10):1196.
- Poveda C, Herreros-Cabello A, Callejas-Hernández F, Osuna-Pérez J, Maza MC, Chillón-Marinas C, Calderón J, Stamatakis K, Fresno M, Gironès N. 2020. Interaction of Signaling Lymphocytic Activation Molecule Family 1 (SLAMF1) receptor with Trypanosoma cruzi is strain-dependent and affects NADPH oxidase expression and activity. PLoS Negl Trop Dis. Sep 14;14(9):e0008608.
- Callejas-Hernández F, Gutiérrez-Nogués Á, Rastrojo A, Gironès N, Fresno M. 2019. Analysis of mRNA processing at whole transcriptome level, transcriptomic profile and genome sequence refinement of Trypanosoma cruzi. Sci Rep. Nov 22;9(1):17376.
- Herreros-Cabello A, Callejas-Hernández F, Fresno M, Gironès N. 2019. Comparative proteomic analysis of trypomastigotes from Trypanosoma cruzi strains with different pathogenicity. Infect Genet Evol. Dec;76:104041.
- Callejas-Hernández C, Rastrojo A, Poveda C, Gironès N and Fresno M. 2018. Genomic assemblies of newly sequenced Trypanosoma cruzi strains reveal new genomic expansion and greater complexity. Sci Rep. Oct 2; 8:14631.
- Carbajosa S, Rodríguez-Angulo HO, Gea S, Chillón-Marinas C, Poveda C, Maza MC, Colombet D, Fresno M, Gironès N. L-arginine supplementation reduces mortality and improves disease outcome in mice infected with Trypanosoma cruzi. PLoS Negl Trop Dis. 2018 Jan 16;12(1):e0006179.
- Cuervo H, Guerrero NA, Carbajosa S, Beschin A, De Baetselier P, Gironès N, Fresno M. Myeloid-derived suppressor cells infiltrate the heart in acute Trypanosoma cruzi infection. J Immunol. 2011 Sep 1;187(5):2656-65. doi: 10.4049/jimmunol.1002928. Epub 2011 Jul 29. PMID: 21804013.
- Cuervo H, Pineda MA, Aoki MP, Gea S, Fresno M, Gironès N. Inducible nitric oxide synthase and arginase expression in heart tissue during acute Trypanosoma cruzi infection in mice: arginase I is expressed in infiltrating CD68+ macrophages. J Infect Dis. 2008 Jun 15;197(12):1772-82.
c Autor para correspondencia. 1 Igual contribución a la dirección del trabajo.




















