Carlos Perea Resa Lab. 409 Ext. 4463
Dinámica y Reciclaje de la maquinaria de transcripción durante mitosis.
Un aspecto fascinante de nuestra biología es el hecho de que todas las células de nuestro organismo comparten la misma información genética (libro de instrucciones). La lectura diferencial de esta información es la clave para generar la diversidad celular durante el desarrollo. En este contexto, la transcripción del DNA a RNA constituye la primera etapa de esa lectura y es fundamental para establecer los patrones de expresión característicos de cada tipo celular. Asimismo, el proceso de mitosis es esencial para conseguir el numero de células necesario para construir un organismo completo y se ha demostrado que el paso a través de mitosis es además necesario para establecer un alto porcentaje de linajes celulares. Sorprendentemente, el proceso de transcripción es silenciado durante el paso por mitosis como consecuencia de la desvinculación generalizada de RNA polimerasas y factores de transcripción de la cromatina. Una vez finalizada la división celular, la transcripción debe reiniciarse inmediatamente para garantizar la viabilidad celular. ¿Cómo las células hijas recuerdan y reestablecen los patrones de transcripción? ¿Cómo los patrones se modifican dentro del proceso de diferenciación celular? Estas son algunas de las preguntas que intentamos responder utilizando modelos de líneas celulares humanas para estudiar el proceso de transcripción durante la mitosis. Uno de nuestros objetivos es determinar la regulación y reciclaje durante el tránsito a través de mitosis de la RNA polimerasa 2, enzima encargada de transcribir todos los genes que codifican proteínas, así como la de un complejo asociado denominado Cohesina. En paralelo, estudiamos el papel de estos procesos en el proceso de diferenciación celular y su potencial implicación en el origen de defectos del desarrollo como las cohesinopatías. Combinando entre otras técnicas el cultivo de líneas celulares, estudios de genómica y proteómica, la tecnología CRISPR y el análisis por microscopía de células vivas, estudiamos la dinámica de esta maquinaria para poder entender cómo son coordinados procesos esenciales como la expresión génica y la división celular durante el desarrollo.
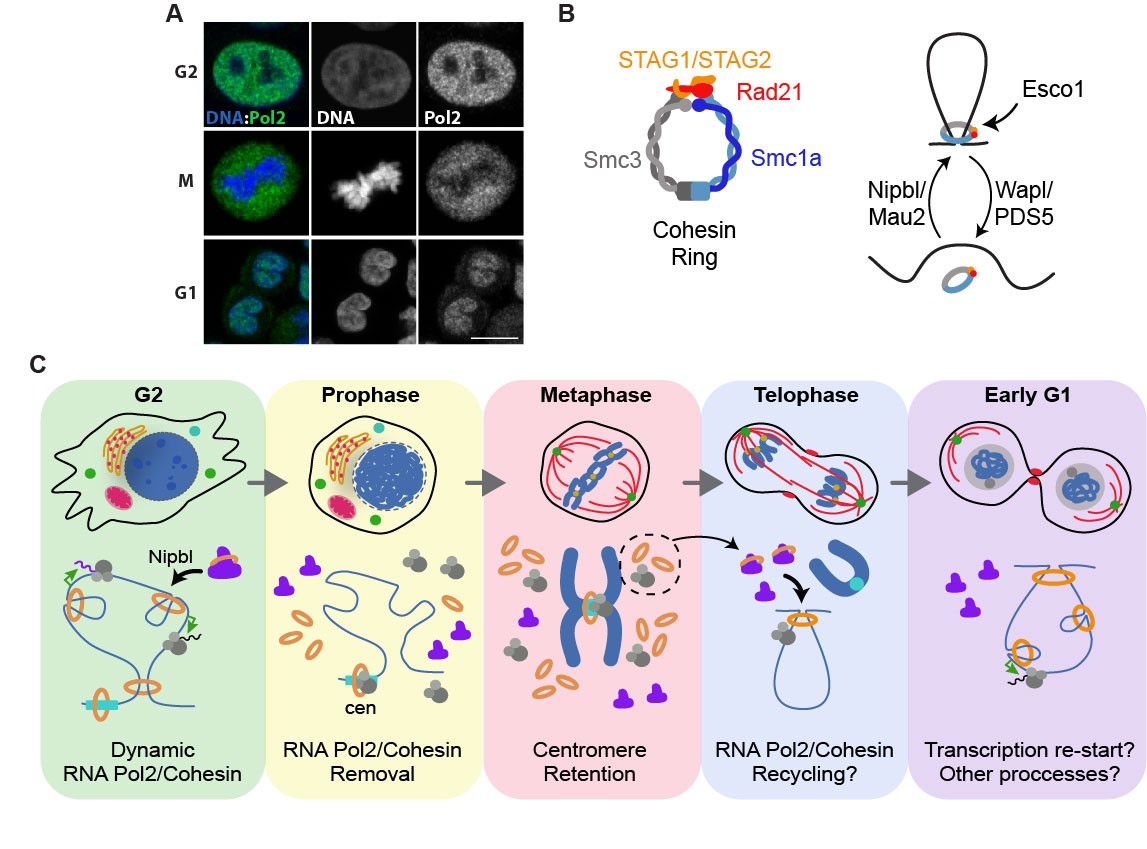
Figura 1. Dinámica y reciclaje de la maquinaria de transcripción durante mitosis. A Análisis de la localización subcelular de la RNA Pol2 en las fases G2, M y G1 del ciclo celular mediante immunofluorescencia. B Esquema de los componentes del complejo Cohesina (izda.) y de los factores implicados en su interacción con la cromatina (derecha). C Modelo representativo de la dinámica y potencial reciclaje de la RNA Pol2 (gris) y cohesina (naranja) durante el paso a través de mitosis.
Twitter: @PereaResa

| Apellidos | Nombre | Laboratorio | Ext.* | Categoría profesional | |
|---|---|---|---|---|---|
| Contreras Pérez | Aida | 322 | 4611 | aida.contreras(at)cbm.csic.es | M3 Predoc.formación |
| García Piñero | María | 409 | 4611 | Estudiante TFM | |
| Perea Resa | Carlos | 409 | 4611 | carlos.perea(at)cbm.csic.es | Doctor FC1 |
| Sayago Pachón | Estrella Isabel | 409 | 4611 | Becario JAE Intro |
1. Perea-Resa C*, Wattendorf L, Marzouk S, and Blower MD*. Trends in Cell Biology, 2021 doi: 10.1016/j.tcb.2021.03.005. *CO-CORRESPONDING AUTHORS
2. Ardehali MB, Damie M, Perea-Resa C, Blower MD and Kingston RE. Journal of Biological Chemistry, 2020. doi: 10.1074/jbc.RA120.015877
3. Hekman RM, Hume AJ, Raghuveera KG, et al., Actionable Cytopathogenic Host Responses of Human Alveolar Type 2 Cells to SARS-CoV-2. Molecular Cell, 2020. doi:10.1016/j.molcel.2020.11.028
4. Sharp JA, Perea-Resa C, Wang W, Blower MD. Cell division requires RNA eviction from condensing chromosomes. Journal of Cell Biology, 2020. doi: 10.1083/jcb.201910148
5. Perea-Resa C, Bury L, Cheeseman IM, Blower MD. Cohesin Removal Reprograms Gene Expression upon Mitotic Entry. Molecular Cell, 2020. doi: 10.1016/j.molcel.2020.01.023
6. Esteve-Bruna D, Carrasco-López C, Blanco-Touriñán N, et al., Prefoldins contribute to maintaining the levels of the spliceosome LSM2-8 complex through Hsp90 in Arabidopsis. Nucleic Acids Research, 2020. doi: 10.1093/nar/gkaa354
7. Perea-Resa C, Blower MD. Centromere Biology: Transcription Goes on Stage. Molecular and Cell Biology, 2018. Review. doi: 10.1128/MCB.00263-18
8. Perea-Resa C, Blower MD. Satellite Transcripts Locally Promote Centromere Formation. Developmental Cell, 2017. doi: 10.1016/j.devcel.2017.07.017
9. Perea-Resa C, Rodríguez-Milla MA, Iniesto E, Rubio V, Salinas J. Prefoldins negatively regulate cold acclimation in Arabidopsis thaliana by promoting nuclear proteasome-mediated HY5 degradation. Molecular Plant, 2017. doi: 10.1016/j.molp.2017.03.012
10. Carrasco-López C, Hernández-Verdeja T, Perea-Resa C, Abia D, Catalá R, Salinas J. Environmental-dependent regulation of spliceosome activity by the LSM2-8 complex in Arabidopsis. Nucleic Acids Research, 2017. doi: 10.1093/nar/gkx375
11. Perea-Resa C, Carrasco-López C, Catalá R, Turečkova V, Novak O, Zhang W, Sieburth L, Jiménez-Gómez JM, Salinas J. The LSM1-7 complex differentially regulates Arabidopsis thaliana tolerance to abiotic stress conditions by promoting selective mRNA decapping. The Plant Cell, 2016. doi: 10.1105/tpc.15.00867
12. Perea-Resa C, Hernández-Verdeja T, López-Cobollo R, del Mar Castellano M, Salinas J. LSM proteins provide accurate splicing and decay of selected transcripts to ensure normal Arabidopsis development. The Plant Cell, 2012. doi: 10.1105/tpc.112.103697




















