Especificación segmental y formación de patrón en Drosophila
Resumen de Investigación:
Una cuestión importante en biología del desarrollo es comprender los mecanismos que regulan el tamaño, la forma y el patrón de las distintas estructuras de un organismo. Queremos estudiar estas cuestiones en Drosophila y basándonos principalmente en el estudio de los genes Hox, los cuales especifican la identidad de distintas estructuras en el eje anteroposterior de todos los organismos bilaterales. Codifican proteínas que se unen al DNA y regulan la expresión de genes que finalmente determinan variaciones en la forma, patrón y tamaño de los órganos.
Estudiamos la diferencia de tamaño y proliferación celular determinada por genes Hox en varios órganos. Investigamos, por ejemplo, como el gen Hox Ultrabithorax reduce el tamaño del metanotum (parte dorsal del tercer segmento torácico, T3) con respecto al del mesonotum (la región dorsal en el segundo segmento torácico, T2, que no expresa Ultrabithorax). En mutantes Ultrabithorax el T3 se transforma en el T2, es decir, Ultrabithorax reduce el tamaño del segmento T3 dorsal. En un análisis similar, queremos conocer los mecanismos por los que los genes Hox regulan una diferente proliferación en los histoblastos, células precursoras del abdomen, o en los discos imaginales, ya que los primeros se dividen fundamentalmente durante la pupa y los segundos durante el periodo larvario. Finalmente, nuestro trabajo se orienta también a conocer las diferencias de tamaño de distintos segmentos que formarán la genitalia. Esta diferente proliferación la establece el gen Hox Abdominal-B en conjunción con los genes que determinan el sexo y está mediada, entre otras, por las vías de señalización de Dpp y Hippo (Fig. 1).
Con respecto al estudio de la determinación de la forma, realizamos un análisis de cómo el gen Ultrabithorax especifica la diferente forma de los halterios (globosos) y las alas (planas). Creemos que esta diferencia se debe cambios en la matriz extracelular en etapas pupales tempranas controlados por Ultrabithorax
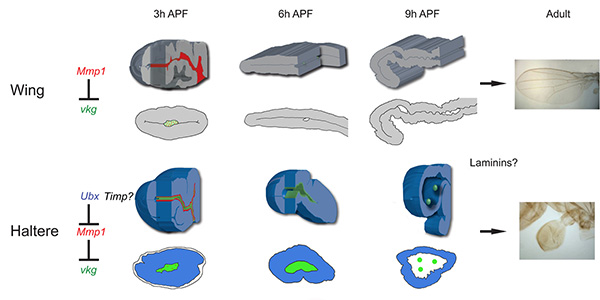
Figura 1. Esquema de expresión de Metaloproteinasa 1 (Mmp1) y colágeno (codificado por el gen viking, vkg) en los discos imaginales de ala y halterio. En este último Ubx impide la aposición de epitelios dorsal y ventral y la forma plana de las alas.
La eliminación de un segmento abdominal
Los machos de Drosophila carecen de segmento séptimo abdominal (A7) mientras que las hembras lo mantienen (aunque reducido). Aunque los histoblastos que dan origen a este segmento están presentes durante el periodo larvario, en la etapa pupal se extruyen en los machos, al igual que las células larvarias, y para este proceso se requiere la actividad del gene Hox Abdominal-B y de los genes de determinación sexual. Queremos estudiar como estos genes regulan el proceso de eliminación de este segmento en un determinado momento de la pupación (vídeo 1). Igualmente analizamos la posible conexión funcional entre la eliminación de este segmento y la rotación de 360º de la placa genital en el macho que tiene lugar en pupa (vídeo 2).
Dado el papel esencial de Abdominal-B en el desarrollo del abdomen posterior y la genitalia, se quiere conocer mejor la relación entre los distintos aminoácidos y motivos conservados de la proteína Abdominal-B y su función, por lo que estudiamos la función de proteínas Abdominal-B mutadas en distintos aminoácidos o motivos conservados en la evolución. En especial analizamos la función de estas proteínas mutadas en el proceso de eliminación del segmento séptimo abdominal en machos, la función de las proteínas Extradenticle y Homothorax en el mismo y la posible interacción de éstas con Abdominal-B.
Vídeo 1. Vídeo que muestra la eliminación de histoblastos del A7 de macho (células pequeñas en las parte superior lateral) y de las células larvarias (grandes, zona central). Los histoblastos del A6 alcanzan la genitalia, que muestra el final de la rotación de 360º (parte superior). Las células están marcadas con neuroglian-GFP.
Vídeo 2. La placa genital rota 360º en pupa. Las células están marcadas con nrg-GFP, en verde, y las células de compartimentos posteriores con hh-Dsred (en rojo).
Regeneración y genes Hox
Los discos imaginales de Drosophila constituyen un buen modelo para estudiar procesos de reprogramación celular. Al dañar o eliminar parte de un disco imaginal, se produce una recuperación del mismo, mediada por distintas señales. Se ha demostrado que durante la regeneración de discos imaginales se producen transgresiones de compartimento, con posibles cambios de identidad celular, incluidos los determinados por genes Hox. Para analizar este punto, estudiamos los cambios de expresión de genes homeóticas que se producen durante la regeneración del disco genital, un disco en el que se distinguen tres segmentos con distinta especificidad homeótica (Fig. 2).
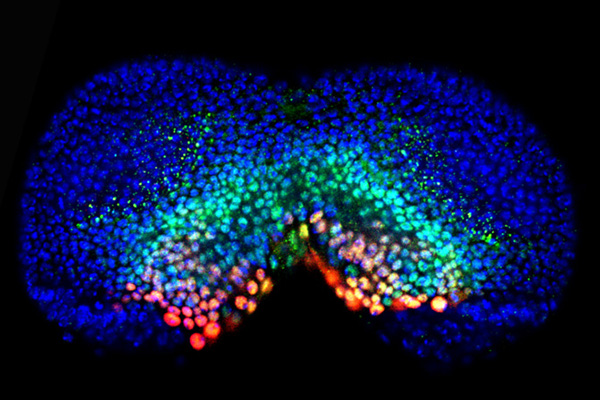
Figura 2. Disco genital de macho en el que se ha inducido muerte en el dominio caudal y se ha dejado regenerar. La expresión de Caudal (en verde) es mas amplia que la de ß-galactosidasa (rojo) que marca el linaje del dominio caudal, sugiriendo que la regeneración tiene lugar con células que no provienen de ese dominio. Topro está en azul.

| Apellidos | Nombre | Laboratorio | Ext.* | Categoría profesional | |
|---|---|---|---|---|---|
| Foronda Alvaro | David | 424 | 4699 | dforonda(at)cbm.csic.es | Tit.Sup.Activ.Técn.y Profes. GP1 66% |
| Martín Fernández | María Paloma | 424 | 4700 | mpmartin(at)cbm.csic.es | E. Técnicos Superiores Especializados de Organismos Públicos de Investigación |
| Sánchez-Herrero Arbide | Ernesto | 424 | 4699 | esherrero(at)cbm.csic.es | E. Profesores de Investigación de Organismos Públicos de Investigación |
| Sánchez Calera | Daniel | 424 | 4700 | Estudiante TFG | |
| Utiel Ortega | Laura | 424 | 4669 | Estudiante TFG |
Publicaciones recientes:
- de Navas, L. F., Garaulet, D. L. y Sánchez-Herrero, E. (2006). The Ultrabithorax Hox gene of Drosophila controls haltere size by regulating de Dpp pathway. Development 133, 4495-4506. http://dev.biologists.org/content/133/22/4495.full.pdf+htm
-
Recomendado en F1000 http://f1000.com/prime/1047077
-
-
Manjón, C., Sánchez-Herrero, E. y Suzanne, M. (2007). Sharp boundaries of Dpp signaling trigger local cell death required for Drosophila leg morphogenesis. Nat.Cell Biol 9, 57-63. http://www.nature.com/ncb/journal/v9/n1/pdf/ncb1518.pdf
-
Comentado en Milán, M. Nat.Cell Biol 9, 17-18 (2007) http://www.nature.com/ncb/journal/v9/n1/pdf/ncb0107-17.pdf y en J. Cell Biol. 176, 4 (2007) http://jcb.rupress.org/content/176/1/4.full.pdf+html
-
- Garaulet, D. L., Foronda, D., Calleja, M. y Sánchez-Herrero, E. (2008). Polycomb-dependent Ultrabithorax Hox gene silencing induced by high Ultrabithorax levels in Drosophila. Development 135, 3219-3228. http://dev.biologists.org/content/135/19/3219.full.pdf+html
-
de Navas, L. F., Reed, H., Akam, M., Barrio, R., Alonso, C.R. y Sánchez-Herrero, E. (2011). Integration of RNA processing and expression level control modulates the function of the Drosophila Hox gene Ultrabithorax during adult development. Development 138, 107-116. http://dev.biologists.org/content/138/1/107.full.pdf+html
-
Foronda, D., Martín, P., y Sánchez-Herrero, E. (2012) Drosophila Hox and sex-determination genes control segment elimination through EGFR and extramacrochetae activity. PLoS Genet. e1002874. doi: 10.1371/journal.pgen.1002874. http://www.ncbi.nlm.nih.gov/pmc/articles/PMC3415437/pdf/pgen.1002874.pdf
-
Curt J. R., de Navas, L. F. y Sánchez-Herrero, E. (2013). Differential activity of Drosophila Hox genes induces myosin expression and can maintain compartment boundaries. PLoS ONE e571. doi: 10.1371/journal.pone.0057159. http://www.ncbi.nlm.nih.gov/pmc/articles/PMC3581558/pdf/pone.0057159.pdf
-
Sánchez-Herrero, E. (2013). Hox targets and cellular functions. Scientifica 738257. doi: 10.1155/2013/73825. http://www.ncbi.nlm.nih.gov/pmc/articles/PMC3892749/pdf/SCIENTIFICA2013-738257.pdf
- Guarner, A., Manjón, C., Edwards, K., Steller, H., Suzanne, M. y Sánchez-Herrero, E. (2014). The zinc finger homeodomain-2 gene of Drosophila controls Notch targets and regulates apoptosis in the tarsal segments. Dev. Biol. 385, 350-365.
- Garaulet, D.L., Castellanos, M.C., Bejarano, F., Sanfilippo, P., Tyler, D.M., Allan, D.W., Sánchez-Herrero, E.* y Lai, E.C*. (2014). Homeotic function of Drosophila Bithorax-Complex miRNAs mediates fertility by restricting multiple Hox genes and TALE cofactors in the central nervous system. Dev. Cell 23, 635-648. doi: 10.1016/j.devcel.2014.04.023. http://www.ncbi.nlm.nih.gov/pubmed/24909902.
-
Recomendado en F1000 http://f1000.com/prime/718442074#recommendations-content
-
- de Navas, L., Foronda, D., Del Saz, D. ¡ Sánchez-Herrero, E. (2014). A genetic strategy to obtain P-Gal4 elements in the Drosophila Hox genes. Methods Mol. Biol. 1196, 49-57. doi: 10.1007/978-1-4939-1242-1_4. http://link.springer.com/protocol/10.1007%2F978-1-4939-1242-1_4.
- Foronda, D., Curt, J.R., Prieto, N., Martín, P. y Sánchez-Herrero, E. (2015). The elimination of an adult segment by the Hox gene Abdominal-B. Mech. Dev. 138, 210-217. doi: 10.1007/978-1-4939-1242-1_4. http://www.sciencedirect.com/science/article/pii/S0925477315300186
- De Las Heras, J. M., García-Cortés, C., Foronda, D., Pastor-Pareja, J. C., Shashidhara, L. S., y Sánchez-Herrero E. (2018). The Drosophila Hox gene Ultrabithorax controls appendage shape by regulating extracellular matrix dynamics. Development 1
- Recomendado en F1000 https://f1000.com/prime/733362447
- Recomendado en F1000 https://f1000.com/prime/733362447
- Romero-Pozuelo, J., Foronda, D., Martín, P., Hudry, B., Merabet, S., Graba, Y. and Sánchez-Herrero E. (2019). Cooperation of axial and sex specific information controls Drosophila female genitalia growth by regulating the Decapentaplegic pathway. Dev. Biol. 454, 145-155. https://www.ncbi.nlm.nih.gov/pubmed/31251896




















