Disfunción mitocondrial en enfermedades metabólicas
Resumen de Investigación:
Las mitocondrias son orgánulos celulares extremadamente complejos que desempeñan funciones esenciales en múltiples aspectos de la biología celular. Si bien en sus inicios se pensaba que su única función era la de generar ATP, hoy es evidente que participan en multitud de procesos celulares como la regulación del balance calcio, la apoptosis, el equilibrio redox o la identidad celular. Debido a lo polifacético que son estos orgánulos y la importancia que tienen en procesos biológicos y metabólicos, no es sorprendente que su disfunción esta ligada a numerosas patologías humanas como enfermedades neurodegenerativas, diabetes, cáncer o envejecimiento. En nuestro laboratorio buscamos entender los componentes moleculares que regulan la función mitocondrial e integrar este conocimiento en diferentes contextos fisiológicos y patológicos.
Actualmente estamos centrando nuestros esfuerzos en dos áreas de investigación especificas. Primero, nos proponemos elucidar los mecanismos moleculares por los cuales la disfunción mitocondrial compromete negativamente la viabilidad celular y debilita el correcto funcionamiento de órganos y tejidos. Segundo, estamos interesados en entender como las células cancerosas reprograman su metabolismo frente a microambientes tumorales desfavorables para aumentar su supervivencia y proliferación.
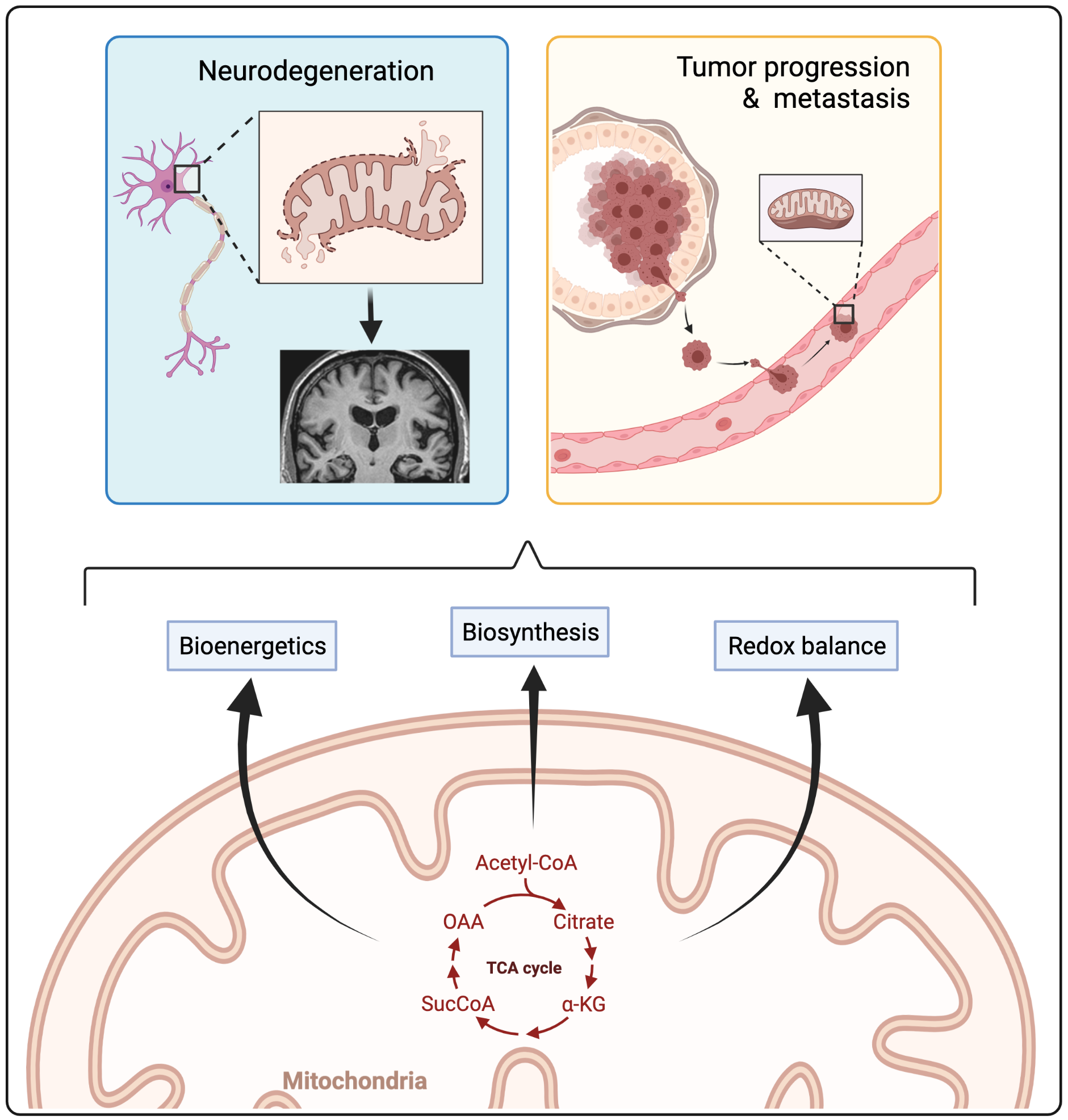
Fig.1: Las mitocondrias catabolizan diversos nutrientes para producir energía (ATP), generan precursores biosintéticos y mantienen la homeostasis redox. Nuestro laboratorio está interesado en estudiar cómo estos procesos metabólicos influyen en procesos patofisiologicos como la neurodegeneración o la progresión tumoral.
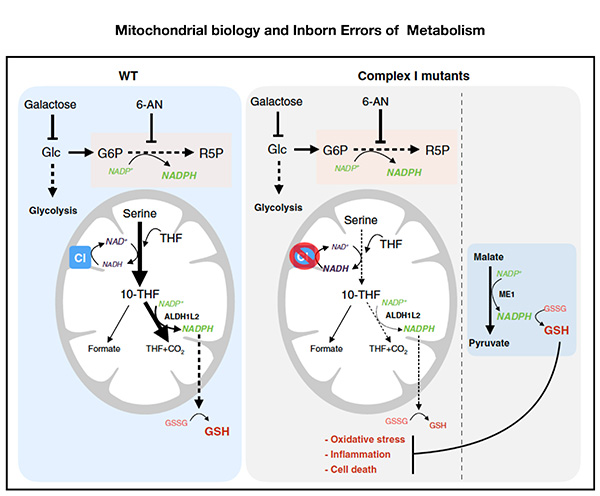
Fig.1: Modelo que ilustra cómo la inhibición del NADPH producido por la via de las pentosas fosfato es compensado por el incremento del “mitochondrial one-carbon metabolism “ y los niveles de la enzima ALDH1L2. Por el contrario, células y tejidos con disfunción mitocondrial tienen comprometido el catabolismo de la serina por esta ruta y la producción asociada de NADPH, lo cual reduce los niveles de GSH y aumenta el estrés oxidativo causando inflamación y muerte celular. La expresión de ME1 incrementa los niveles de NADPH y es capaz de corregir este desequilibrio redox lo que puede representar una opción terapéutica para enfermedades asociadas con la disfunción mitocondrial que cursan con elevados niveles de estrés oxidativo.
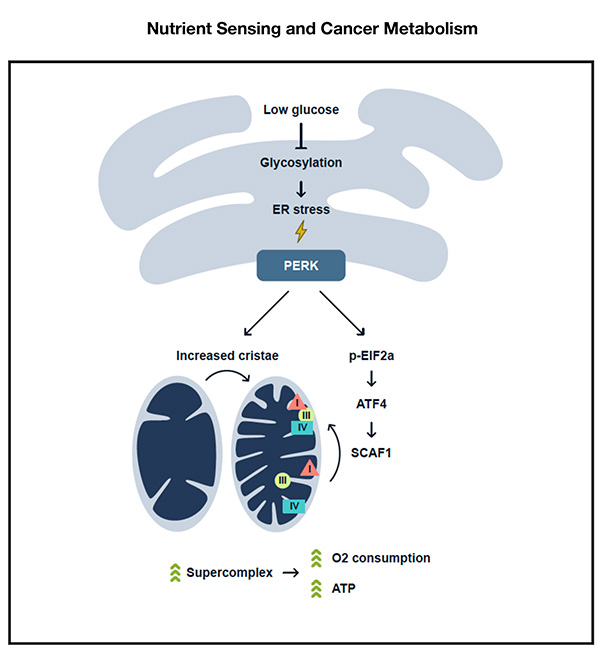
Fig. 2: Nuestras investigaciones han elucidado el mecanismo por el cual la deprivación de glucosa activa la generación de ATP mitocondrial. Cuando la glucosa es limitante, la quinasa PERK se activa y estimula la formación de crestas mitocondriales. En paralelo el eje PERK-eIF2a-ATF4 incrementa los niveles de SCAF1 para asistir a la formación de los supercomplejos de la cadena de transporte de electrones mitocondrial. Todo este programa tiene como finalidad estimular el sistema OXPHOS e incrementar la produción de ATP mitocondrial en condiciones en las que la glucólisis esta reducida a consecuencia de una falta en el aporte de glucosa.

| Apellidos | Nombre | Laboratorio | Ext.* | Categoría profesional | |
|---|---|---|---|---|---|
| Balsa Martínez | Eduardo | 427 | 4739 | ebalsa(at)cbm.csic.es | Investigador Doctor |
| Castillo Serrulla | Pablo | 427 | 4740 | pcastillo(at)cbm.csic.es | Titulado Sup.de Actividades Técn. y Profes. GP1 |
| Cruz Vilchez | Víctor Manuel | 427 | 4739 | vmcruz(at)cbm.csic.es | M3 Predoc.formación |
| Jaraíz Rodríguez | Miriam | 427 | 4739 | mjaraiz(at)cbm.csic.es | Titulado Superior Grado de Doctor |
| Laine Menéndez | Sara | 427 | 4740 | sara.laine(at)cbm.csic.es | Investigador Doctor |
| Losada de Paz | Raquel | 427 | 4740 | rlosada(at)cbm.csic.es | Titulado Sup.de Actividades Técn. y Profes. GP1 |
| Pozo Ramos | Natalia del | 427 | 4740 | ndelpozo(at)cbm.csic.es | Tco. de Investigación y Laboratorio |
| Prado Montero | Lucía del | 427 | 4740 | ldelprado(at)cbm.csic.es | Titulado Sup.de Actividades Técn. y Profes. GP1 |
| Roca Portoles | Alba | 427 | 4740 | alba.roca(at)cbm.csic.es | Investigador Doctor |
| Zamora Dorta | Marcos Javier | 427 | 4740 | mzamora(at)cbm.csic.es | Contrato Predoctoral |
Publicaciones relevantes:
- Balsa E, Perry EA, Bennett CF, Jedrychowski M, Gygi SP, Doench J, Puigserver P. Defective NADPH Production in Mitochondrial Disease Complex I Causes Inflammation and Cell Death. Nature Communications. 2020.
- Luo C, Balsa E, Perry EA, Liang J, Tavares CD, Vazquez F, Widlund HR, Puigserver P. H3K27me3-mediated PGC1α gene silencing promotes melanoma invasion through WNT5A and YAP. J Clin Invest. 2020 Jan 13. pii: 130038.
- Balsa E, Soustek MS, Thomas A, Cogliati S, Garcia-Poyatos C, Martin-Garcia E, Jedrychowski M, Gygi SP, Enríquez JA, Puigserver P. ER and Nutrient Stress Promote Assembly of Respiratory Chain Supercomplexes Through PERK/eIF2α Axis. Mol Cell. 2019. Jun 6;74(5):877-890.
- Soustek MS, Balsa E, Barrow JJ, Jedrychowski M, Vogel R, Jan Smeitink, Gygi SP, Puigserver P. Inhibition of the ER stress IRE1α inflammatory pathway protects against cell death in mitochondrial complex I mutant cells. Cell Death Dis. 2018 May 31;9(6):658.
- Luo C, Balsa E, Thomas A, Hatting M, Jedrychowski M, Gygi SP, Widlund HR, Puigserver P. ERRα Maintains Mitochondrial Oxidative Metabolism and Constitutes an Actionable Target in PGC1α-Elevated Melanomas. Mol Cancer Res. 2017 Oct;15(10):1366-1375
- Barrow JJ*, Balsa E*, Verdeguer F, Tavares CDJ, Soustek MS, Hollingsworth IV LR, Jedrychowski M, Vogel R, Paulo J, Smeitink J, Gygi S, Doench J, Root D, Puigserver P. Bromodomain Inhibitors Correct Bioenergetic Deficiency Caused by Mitochondrial Disease Complex I Mutations. Mol Cell 2016. Oct 6; 64(1): 163-175. (*Co-first author).
- Soro-Arnaiz I, Li QOY, Torres-Capelli M, Meléndez-Rodríguez F, Veiga S, Veys K, Sebastian D, Elorza A, Tello D, Hernansanz-Agustín P, Cogliati S, Moreno-Navarrete JM, Balsa E, Fuertes E, Romanos E, Martínez-Ruiz A, Enriquez JA, Fernandez-Real JM, Zorzano A, De Bock K, Aragonés J. Role of Mitochondrial Complex IV in Age-Dependent Obesity. Cell Rep. 2016 Sep 13;16(11):2991-3002.
- Lapuente-Brun E, Moreno-Loshuertos R, Acín-Pérez R, Latorre-Pellicer A, Colás C, Balsa E, Perales-Clemente E, Quirós PM, Calvo E, Rodríguez-Hernández MA, Navas P, Cruz R, Carracedo Á, López-Otín C, Pérez-Martos A, Fernández-Silva P, Fernández-Vizarra E, Enríquez JA. Supercomplex assembly determines electron flux in the mitochondrial electron transport chain. Science. 2013 Jun 28;340(6140):1567-70
- Balsa E, Marco R, Perales-Clemente E, Szklarczyk R, Calvo E, Landázuri MO, Enríquez JA. NDUFA4 is a subunit of complex IV of the mammalian electron transport chain. Cell Metab. 2012 Sep 5;16(3):378-86
- Tello D*, Balsa E*, Acosta-Iborra B, Fuertes-Yebra E, Elorza A, Ordóñez Á, Corral-Escariz M, Soro I, López-Bernardo E, Perales-Clemente E, Martínez-Ruiz A, Enríquez JA, Aragonés J, Cadenas S, Landázuri MO. Induction of the mitochondrial NDUFA4L2 protein by HIF-1α decreases oxygen consumption by inhibiting Complex I activity. Cell Metab. 2011 Dec 7;14(6):768-79. (*Co-first author).
Financiación:
- Ministerio de Ciencia e Innovación (MICINN):
- Ramón y Cajal 2018 (RYC2018-024342-I)
- Programa Estatal de I+D+i (PID2019-110766GA-I00)
- EC-European Research Council:
- ERC Starting Grant (2020 ERC-Stg) 948478 MitoCure




















