Grupo redes de señalización celular en cáncer (onco-resecel)
Resumen de Investigación:
El cáncer de mama es una enfermedad de alta prevalencia con 25.000 casos diagnosticados en España cada año. Su incidencia es mucho mayor en el mundo desarrollado, sugiriendo que el estilo de vida occidental con hábitos alimenticios poco saludables (ingesta calórica excesiva, sobrepeso, obesidad) y estados de estrés crónico (sobre-estimulación adrenérgica) pueden influir en la aparición y progresión de esta enfermedad.
La variedad histopatológica y heterogeneidad molecular de los tumores de mama (subtipos luminales, triple negativo, ERBB2), junto con la inestabilidad genómica y diversidad celular dentro de cada tumor, son factores que dificultan el tratamiento. En el cáncer de mama las principales proteínas alteradas y responsables de la inestabilidad genómica y heterogeneidad son la quinasa ATM, la ligasa Brca1 y el factor supresor de tumores p53, junto con su regulador negativo la ligasa Mdm2. Aunque en el ~80% de los carcinomas ductales de mama, p53 está neutralizado por la activación/amplificación de Mdm2 o por la desactivación de reguladores positivos como ATM, las terapias basadas en estas dianas no son aún satisfactorias.
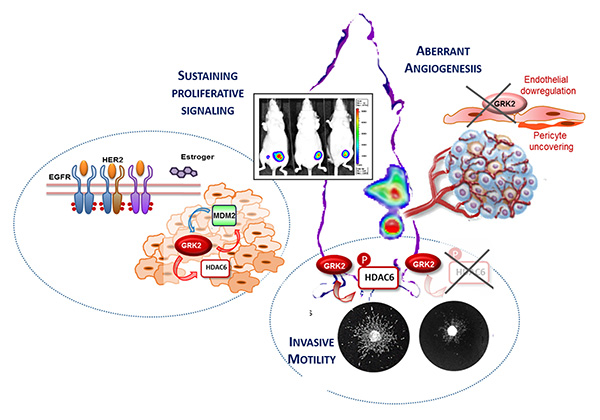
Fig 1. El eje Mdm2/GRK2/HDAC6 desempeña un papel clave en la progresión del cáncer de mama. La activación interdependiente de estos nodos de señalización promueve la tumorogénesis de la mama a través de la estimulación de angiogénesis pro-tumoral, la proliferación celular, la invasión y la metástasis.
Sin embargo, la identificación de dependencias moleculares en ciertos subtipos de cáncer de mama ha mejorado el tratamiento de pacientes con tumores ERBB2(Her2)+ o luminales mediante fármacos dirigidos contra el receptor tirosina-quinasa HER2 o los receptores de estrógeno (ER). Sin embargo, en los tumores “triple negativo” (TNBCs) (negativos para el receptor de estógenos (ER), de progesterona (PR) y el receptor ERBB2) no hay dependencias claramente identificadas, y los tratamientos son poco eficaces. Otro problema importante es el desarrollo de resistencias en el cáncer de mama luminal, Her2 y triple negativo, en paralelo a la heterogeneidad causada por la inestabilidad genómica y la reprogramación metabólica tumoral.
El objetivo de nuestro grupo es identificar, como potenciales dianas terapéuticas multifuncionales, nodos de señalización que cooperen con oncogenes en la adquisición de capacidades tumorales (angiogénesis, proliferación, invasión o metástasis) o que bloqueen la actividad de supresores tumorales, pudiendo alterar la homeostasis celular.
Resultados de nuestro laboratorio sugieren que la alteración coordinada de la serina-treonina quinasa GRK2 y la ligasa Mdm2 es importante en la transformación autónoma de las células, así como en la interrelación de la célula transformada con el micro-ambiente tumoral y el estado sistémico del paciente. Nuestros resultados indican que estas proteínas se modulan mutuamente de manera diferente en células epiteliales normales y en células tumorales, respondiendo distintamente a señales que estimulan receptores adrenérgicos y otros receptores acoplados a proteínas G (GPCR), o receptores tirosina-quinasa de factores de crecimiento (RTK).
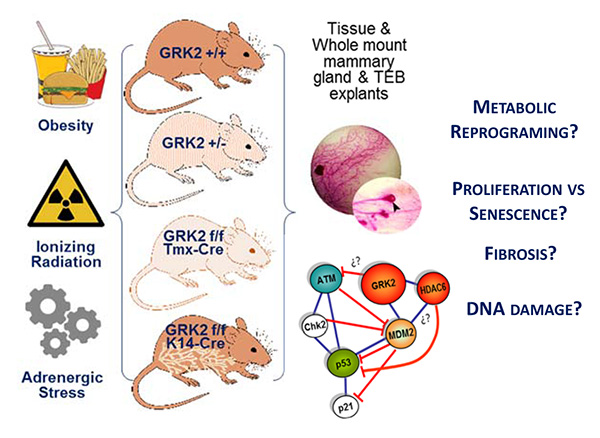
Fig. 2. Modelos animales para estudiar el papel del eje GRK2/Mdm2 en la influencia de diversos factores ambientales de estrés en la progresión tumoral.
En este contexto, nuestras líneas de investigación se centran en caracterizar estos nodos (GRK2 y Mdm2), y las proteínas que modifican por fosforilación y ubiquitinación, en a) procesos celulares como el control de ciclo celular y división celular, diferenciación, metabolismo energético o senescencia que son clave para el mantenimiento de la normalidad celular; b) las consecuencias del estrés hormonal (adrenérgico, estrogénico) y metabólico en la estabilidad genómica; y c) el remodelado pro-tumoral del estroma mamario analizando angiogenesis patológica y la fibrosis que facilitan el crecimiento y diseminación del tumor.
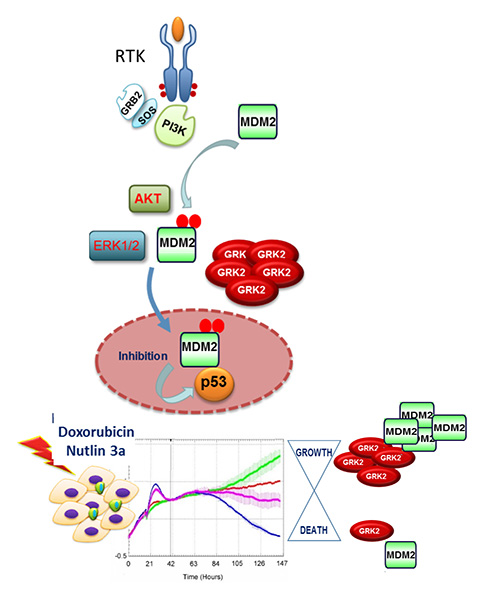
Fig. 3. La coincidente regulación al alza de GRK2 y Mdm2 es una característica de las células epiteliales tumorales de la mama, particularmente en el subtipo luminal positivo para receptores hormonales, que confiere quimioresistencia celular.

| Apellidos | Nombre | Laboratorio | Ext.* | Categoría profesional | |
|---|---|---|---|---|---|
| Arroba Gallego | Javier | 320 | 911964652 | Estudiante TFM | |
| García Mateos | Dafne | 304 | 4656 | dafne.garcia(at)cbm.csic.es | Titulado Sup.Inv.y Laboratorio |
| González Muñoz | Teresa | 320 | 4652 | Investigador Indef. GP1 | |
| Moyano Jimeno | Clara | 320 | 4652 | cmoyano(at)cbm.csic.es | Titulado Sup.Inv.y Laboratorio |
| Nogués Vera | Laura | 320 | 4640 | lnogues(at)cbm.csic.es | Profesor Ayudante Doctor Universidad |
| Penela Márquez | Petronila | 320 | 4640 | ppenela(at)cbm.csic.es | Profesor Titular Universidad, GA |
| Rodríguez Blanco | Clara | 320 | 4652 | Estudiante TFG | |
| Vázquez de Oro | Estefanía | 320 | 4652 | evazquez(at)cbm.csic.es | Tco. de Investigación y Laboratorio |
Publicaciones relevantes:
- P Penela; J Inserte; P Ramos; D García-Dorado; F Mayor Jr. Degradation of GRK2 and AKT is an early and detrimental event in ischemia/reperfusion. EbioMedicine (2019) in press
- P Penela; C Ribas; F Sánchez-Madrid; F Mayor Jr. G protein-coupled receptor kinase 2 (GRK2) as a multifunctional signaling hub. Cellular and Molecular Life Sciences (2019) doi: 10.1007/s00018-019-03274-3
- D Aluja; J Inserte J; P Penela; P Ramos; C Ribas; MA Iñiguez; F Mayor Jr; D Garcia-Dorado. Calpains mediate isoproterenol-induced hypertrophy through modulation of GRK2. Basic Research in Cardiology (2019) 114: 21 (1-14)
- L Nogués; J Palacios-García; C Reglero; V Rivas; M Neves; C Ribas; P Penela; F Mayor. G protein-coupled receptor kinases (GRKs) in tumorigenesis and cancer progression: GPCR regulators and signaling hubs. Seminars in Cancer Biology. (2018) S1044-579X(17)
- L. Nogués, C. Reglero, V. Rivas, M. Neves, P. Penela and F. Mayor Jr. G protein-coupled receptor kinase 2 (GRK2) as a potential modulator of the hallmarks of cancer. Mol. Pharmacol. (2017) 91: 220-228
- L. Nogués, C. Reglero, V. Rivas, A. Salcedo, V. Lafarga, M. Neves, P. Ramos , M. Mendiola, A. Berjón, K. Stamatakis, X. Z. Zhou, K. P. Lu, D.Hardisson, F. Mayor, jr., and P.Penela. G protein-coupled receptor kinase 2 (GRK2) promotes breast tumorigenesis through a novel HDAC6-Pin1 axis. EBioMedicine (2016) 13: 132-145
- P. Penela. Ubiquitination and Protein Turnover of G Protein coupled Receptor Kinases in GPCR Signaling and Cellular Regulation. Progress in Molecular Biology and Translation Science (2016) 141: 85-140
- V. Rivas, L. Nogués, C. Reglero, F. Mayor .Jr. and P. Penela. Role of G protein-coupled receptor kinase 2 in tumoural angiogenesis Mol. Cell. Oncol. (2014) e969166-1-11
- Fernández-Arenas E, Calleja E, Martínez-Martín N, Gharbi SI, Navajas R, García-Medel N, Penela P, Alcamí A, Mayor F Jr, Albar JP, Alarcón B.β-Arrestin-1 mediates the TCR-triggered re-routing of distal receptors to the immunological synapse by a PKC-mediated mechanism. EMBO J.(2014) 33: 559-577
- P. Penela, L. Nogués, and F. Mayor Jr. Roles of GRKs in cell migration. Curr. Opin. Cell Biol. (2014) 27: 10-17
- V. Rivas , R. Carmona ., R. Muñoz-Chápuli, M. Mendiola, L. Nogués, C. Reglero, M. Miguel-Martín, R. García-Escudero, G. W Dorn II, D. Hardisson, F. Mayor, jr. and P. Penela. Developmental and tumoural vascularization is regulated by G-protein-coupled receptor kinase 2. J. Clin. Invest (2013) 123: 4714-4730
Tesis doctorales:
- Verónica Rivas Guerrero (2018) “Caracterización del papel funcional de GRK2 en la fisiología del endotelio y en los procesos vasculares de angiogénesis y vasculogénesis”
- Clara Reglero Gomez (2017) “Regulation of GRK2 by Mdm2 and the APC/C complex: a way to fine-tune dynamics and faithful progression of the cell cycle”
- Laura Nogués Vera (2014) “GRK2 as a new onco-modulator of breast tumoural transformation through the regulation of the p53/MDM2 axis”




















