Programa Científico
Dinámica y función del genoma
GRUPO DE INVESTIGACIÓN
Iniciación interna de la traducción en mRNAs eucarióticos

Encarna Martinez-Salas
Nuestro grupo pretende comprender la conexión entre RNA y proteínas de interacción con RNA en regulación de la traducción. Hemos identificado el dominio de dimerización y el de interacción con RNA de Gemin5, una proteína multifuncional implicada en splicing y traducción. Esta información es esencial para investigar procesos interrumpidos por mutaciones bialélicas en el Gemin5 encontradas en pacientes que sufren enfermedades neurológicas.
Investigación
Nuestros objetivos se centran en comprender los principios que guían los mecanismos alternativos de iniciación de la traducción en eucariotas a través de la caracterización de proteínas de unión a ARN (RBPs) que interactúan con ARNm. Los sitios internos de entrada al ribosoma (IRES) son regiones de ARN no codificante que sustituyen la función de la caperuza terminal 5′ de los ARNm, el punto de anclaje de la maquinaria de traducción. Nuestros estudios han permitido identificar las proteínas que modulan la actividad de los IRES y comprender las restricciones estructurales que son esenciales para su actividad. Hemos demostrado que Gemin5 interactúa con IRES virales, así como con un grupo selectivo de ARNm celulares. Gemin5 es una proteína multitarea que forma parte del complejo de supervivencia de la motoneurona (SMN) y también desempeña una función reguladora de la traducción. El dominio N-terminal de Gemin5 participa en la interacción con el ribosoma y los snRNAs, mientras que la región C-terminal alberga un módulo de dimerización y un sitio no convencional de unión a ARN (RBS). El dominio de dimerización consiste en un dominio similar al tetratricopéptido (TPR) que se autoensambla en un dímero con forma de canoa.
La alteración de la capacidad de dimerización de Gemin5 anula la mejora de la traducción inducida por el fragmento C-terminal de la proteína. La fracción RBS alberga una región intrínsecamente desordenada (IDR) que coevolucionó con la región de interacción ARN, revelando la selección evolutiva del módulo de interacción ARN-proteína. La identificación de los socios ARN del dominio RBS desveló un bucle de retroalimentación con su propio ARNm, contrarrestando el efecto negativo de Gemin5 sobre la traducción. En particular, las variantes de Gemin5 halladas recientemente en pacientes con trastornos neurológicos albergan defectos estructurales que perjudican la dimerización, reducen la traducción y muestran una fuerte disminución del interactoma proteico. En resumen, esta proteína proporciona una importante plataforma para las interacciones RNP, controlando la traducción de ARNm selectivos, incluyendo proteína ribosomal e histonas, críticas para el crecimiento celular, además de ser un actor clave en el ensamblaje del espliceosoma.
Miembros del grupo

Encarnación Martínez Salas
Lab.: 309 Ext.: 4619
emartinez(at)cbm.csic.es

Jorge Ramajo Alonso
Lab.: 309 Ext.: 4649
j.ramajo(at)csic.es

Salvador Abellán Pérez
Lab.: 309 Ext.: 4649
sabellan(at)cbm.csic.es

Azadeh Nahavandi Araghi
Lab.: 309 Ext.: 4619
Publicaciones representativas

Structural basis for the dimerization of Gemin5 and its role in protein recruitment and translation control
María Moreno-Morcillo et al.
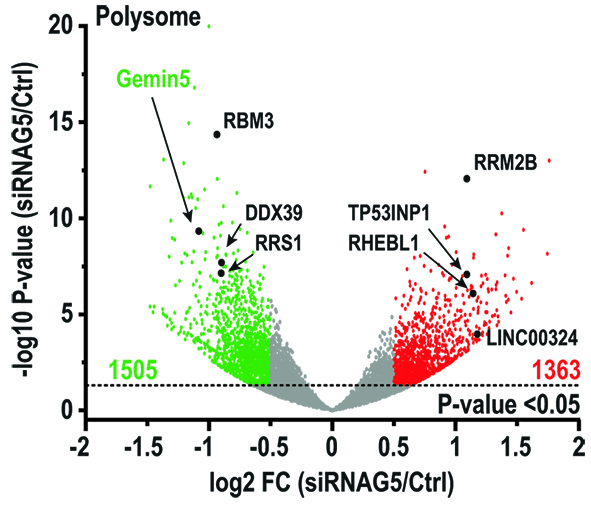
Gemin5-dependent RNA association with polysomes enables selective translation of ribosomal and histone mRNAs
Azman Embarc-Buh et al.
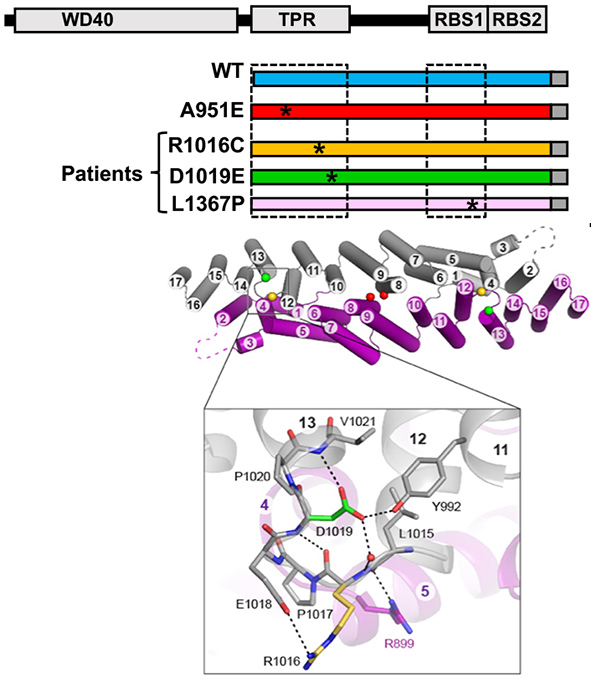
Functional and structural deficiencies of Gemin5 variants associated with neurological disorders
Rosario Francisco-Velilla et al.

Structural basis for Gemin5 decamer-mediated mRNA binding
Qiong Guo et al.