Programa Científico
Interacciones con el entorno
UNIDADES EN ESTE PROGRAMA
Microorganismos en la salud y el bienestar Desarrollo y función del sistema inmunitario
GRUPO DE INVESTIGACIÓN
Interacción virus-célula. El modelo del VPPA

Yolanda Revilla
El laboratorio de la Dra. Revilla estudia distintos aspectos moleculares de la interacción del virus de la peste porcina africana (VPPA) con su célula diana, abordando los mecanismos del tropismo, los genes de virulencia y el control viral del sistema inmune. Esto nos ha permitido la generación de candidatos vacunales mediante CRISPR/Cas9. El VPPA representa la mayor pandemia animal en todo el mundo, y urge el desarrollo de vacunas seguras y eficaces.
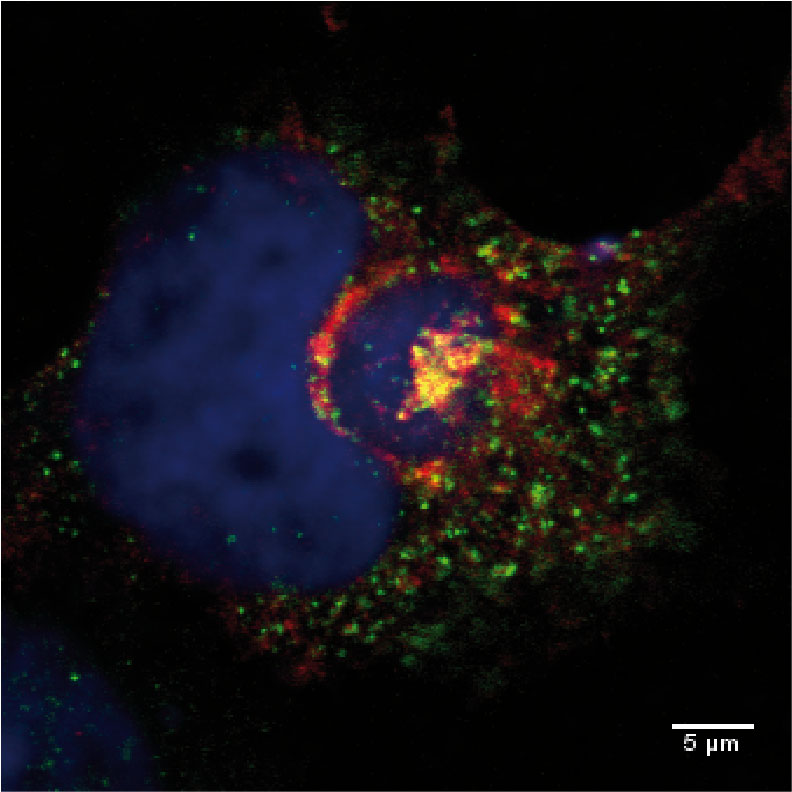
Investigación
El laboratorio del Virus de la peste porcina africana (VPPA) dirigido por la Dr. Yolanda Revilla, estudia los complejos mecanismos virales y celulares que se producen durante la infección del VPPA. La célula diana natural de este virus son exclusivamente los monocitos y macrófagos porcinos, por lo que los factores tanto virales como celulares que determinan su tropismo son un foco de atención en nuestro laboratorio. Otro de los objetivos relevante lo constituyen los mecanismos moleculares implicados en la virulencia del VPPA, que están directamente relacionados con el control que el virus ejerce sobre distintas ramas de la respuesta inmune del animal infectado, y, en particular, sobre la respuesta innata regulando el IFN de tipo I, como hemos descrito en el grupo. Además, estamos interesados en generar candidatos vacunales frente al VPPA basados, fundamentalmente, en vacunas vivas atenuadas (LAVs) y muy recientemente, también basados en prototipos sólo parcialmente replicativos, lo que constituye una primicia en el campo y sería un gran avance por su seguridad. Para ello, abordamos el estudio de la interacción virus-huésped mediante técnicas de biología celular, bioquímicas, microscopía y citometría, junto con la generación de virus recombinantes mediante la tecnología CRISPR-Cas9 (adaptada a la biología del virus por el Dr. Daniel Pérez Núñez, postdoc senior en el grupo), así como su caracterización genética con técnicas NGS como Illumina y Nanopore. Colaboramos además activamente con otros centros de investigación y empresas, tanto en España como en Europa y Asia, para analizar y evaluar el comportamiento del VPPA in vivo, así como la respuesta inmune protectora de los distintos prototipos vacunales.
El VPPA infecta cerdos domésticos y jabalíes y constituye en la actualidad la gran pandemia animal, siendo el mayor problema de la industria porcina mundial además de ser el responsable de un gran desastre ecológico. Desde 2007 un brote en el Cáucaso, el VPPA se fue extendiendo por Rusia hacia Europa del este, y en la actualidad está muy extendido por Europa, Asia (en particular China) y África, donde es endémico, además de estar presente en Oceanía y el Caribe, amenazando seriamente con continuar su expansión por América. Los estudios moleculares de la interacción virus-célula, así como la generación de prototipos vacunales, contribuirán en el medio y largo plazo a contener y prevenir la gran amenaza que en la actualidad supone el VPPA.
Miembros del grupo

Yolanda Revilla Novella
Lab.: 225 Ext.: 4570
yrevilla(at)cbm.csic.es

Daniel Pérez Núñez
Lab.: 225 Ext.: 4598
daniel_perez(at)cbm.csic.es

Gonzalo Vigara Astillero
Lab.: 225 Ext.: 4598
gvigara(at)cbm.csic.es

Roberta Piredda
Lab.: 225 Ext.: 4598
rpiredda(at)cbm.csic.es

Julia Gata de Benito
Lab.: 225 Ext.: 4598
julia.gata(at)cbm.csic.es

Raúl Díaz Subero
Lab.: 225 Ext.: 4598
raul.diaz(at)cbm.csic.es

María Mercedes Montón Peco
Lab.: 225 Ext.: 4598
mmonton(at)cbm.csic.es
Publicaciones representativas
African Swine Fever Virus Uses Macropinocytosis to Enter Host Cells
Elena G. Sánchez et al.

African Swine Fever Virus Armenia/07 Virulent Strain Controls Interferon Beta Production through the cGAS-STING Pathway
Raquel García-Belmonte et al.

Recombinant African Swine Fever Virus Arm/07/CBM/c2 Lacking CD2v and A238L Is Attenuated and Protects Pigs against Virulent Korean Paju Strain
Daniel Pérez-Núñez et al.

Signal peptide and N-glycosylation of N-terminal-CD2v determine the hemadsorption of African swine fever virus
Daniel Pérez-Núñez et al.