Programa Científico
Procesos fisiológicos y patológicos
UNIDADES EN ESTE PROGRAMA
Neuropatología molecular Redes metabólicas y señalizadoras en la enfermedad
GRUPO DE INVESTIGACIÓN
Redes de señalización celular en el cáncer (onco-resecel)

Petronila Penela Márquez
El cáncer causa mortalidad por la progresión metastásica y resistencia a terapias. Nuestro enfoque es entender cómo el estrés y la obesidad influyen en estos procesos, centrándonos en cambios del ciclo celular, identidad celular, angiogénesis y microambientes permisivos, mediante recableado postraduccional de la señalización por quinasas y ligasas en la mama, células tumorales de mama y endotelio

Investigación
El cáncer de mama es una enfermedad de alta prevalencia con 25.000 casos diagnosticados en España cada año. Su incidencia es mucho mayor en el mundo desarrollado, sugiriendo que el estilo de vida occidental con hábitos alimenticios poco saludables (ingesta calórica excesiva, sobrepeso, obesidad) y estados de estrés crónico (sobre-estimulación adrenérgica) pueden influir en la aparición y progresión de esta enfermedad.
La variedad histopatológica y heterogeneidad molecular de los tumores de mama (subtipos luminales, triple negativo, ERBB2), junto con la inestabilidad genómica y diversidad celular dentro de cada tumor, son factores que dificultan el tratamiento. En el cáncer de mama las principales proteínas alteradas y responsables de la inestabilidad genómica y heterogeneidad son la quinasa ATM, la ligasa Brca1 y el factor supresor de tumores p53, junto con su regulador negativo la ligasa Mdm2. Aunque en el ~80% de los carcinomas ductales de mama, p53 está neutralizado por la activación/amplificación de Mdm2 o por la desactivación de reguladores positivos como ATM, las terapias basadas en estas dianas no son aún satisfactorias.
Sin embargo, la identificación de dependencias moleculares en ciertos subtipos de cáncer de mama ha mejorado el tratamiento de pacientes con tumores ERBB2(Her2)+ o luminales mediante fármacos dirigidos contra el receptor tirosina-quinasa HER2 o los receptores de estrógeno (ER). Sin embargo, en los tumores “triple negativo” (TNBCs) (negativos para el receptor de estógenos (ER), de progesterona (PR) y el receptor ERBB2) no hay dependencias claramente identificadas, y los tratamientos son poco eficaces. Otro problema importante es el desarrollo de resistencias en el cáncer de mama luminal, Her2 y triple negativo, en paralelo a la heterogeneidad causada por la inestabilidad genómica y la reprogramación metabólica tumoral.
El objetivo de nuestro grupo es identificar, como potenciales dianas terapéuticas multifuncionales, nodos de señalización que cooperen con oncogenes en la adquisición de capacidades tumorales (angiogénesis, proliferación, invasión o metástasis) o que bloqueen la actividad de supresores tumorales, pudiendo alterar la homeostasis celular.
Resultados de nuestro laboratorio sugieren que la alteración coordinada de la serina-treonina quinasa GRK2 y la ligasa Mdm2 es importante en la transformación autónoma de las células, así como en la interrelación de la célula transformada con el micro-ambiente tumoral y el estado sistémico del paciente. Nuestros resultados indican que estas proteínas se modulan mutuamente de manera diferente en células epiteliales normales y en células tumorales, respondiendo distintamente a señales que estimulan receptores adrenérgicos y otros receptores acoplados a proteínas G (GPCR), o receptores tirosina-quinasa de factores de crecimiento (RTK).
En este contexto, nuestras líneas de investigación se centran en caracterizar estos nodos (GRK2 y Mdm2), y las proteínas que modifican por fosforilación y ubiquitinación, en a) procesos celulares como el control de ciclo celular y división celular, diferenciación, metabolismo energético o senescencia que son clave para el mantenimiento de la normalidad celular; b) las consecuencias del estrés hormonal (adrenérgico, estrogénico) y metabólico en la estabilidad genómica; y c) el remodelado pro-tumoral del estroma mamario analizando angiogenesis patológica y la fibrosis que facilitan el crecimiento y diseminación del tumor.
Miembros del grupo

Laura Nogués Vera
Lab.: 320 Ext.: 4640
lnogues(at)cbm.csic.es

Petronila Penela Márquez
Lab.: 320 Ext.: 4640
ppenela(at)cbm.csic.es

Teresa González Muñoz
Lab.: 320 Ext.: 4652
teresa.gonzalez(at)cbm.csic.es

Clara Moyano Jimeno
Lab.: 320 Ext.: 4652
cmoyano(at)cbm.csic.es

Yazi Xu
Lab.: 320 Ext.: 4652

Ana Isabel Espinosa López
Lab.: 320 Ext.: 4640
Publicaciones representativas
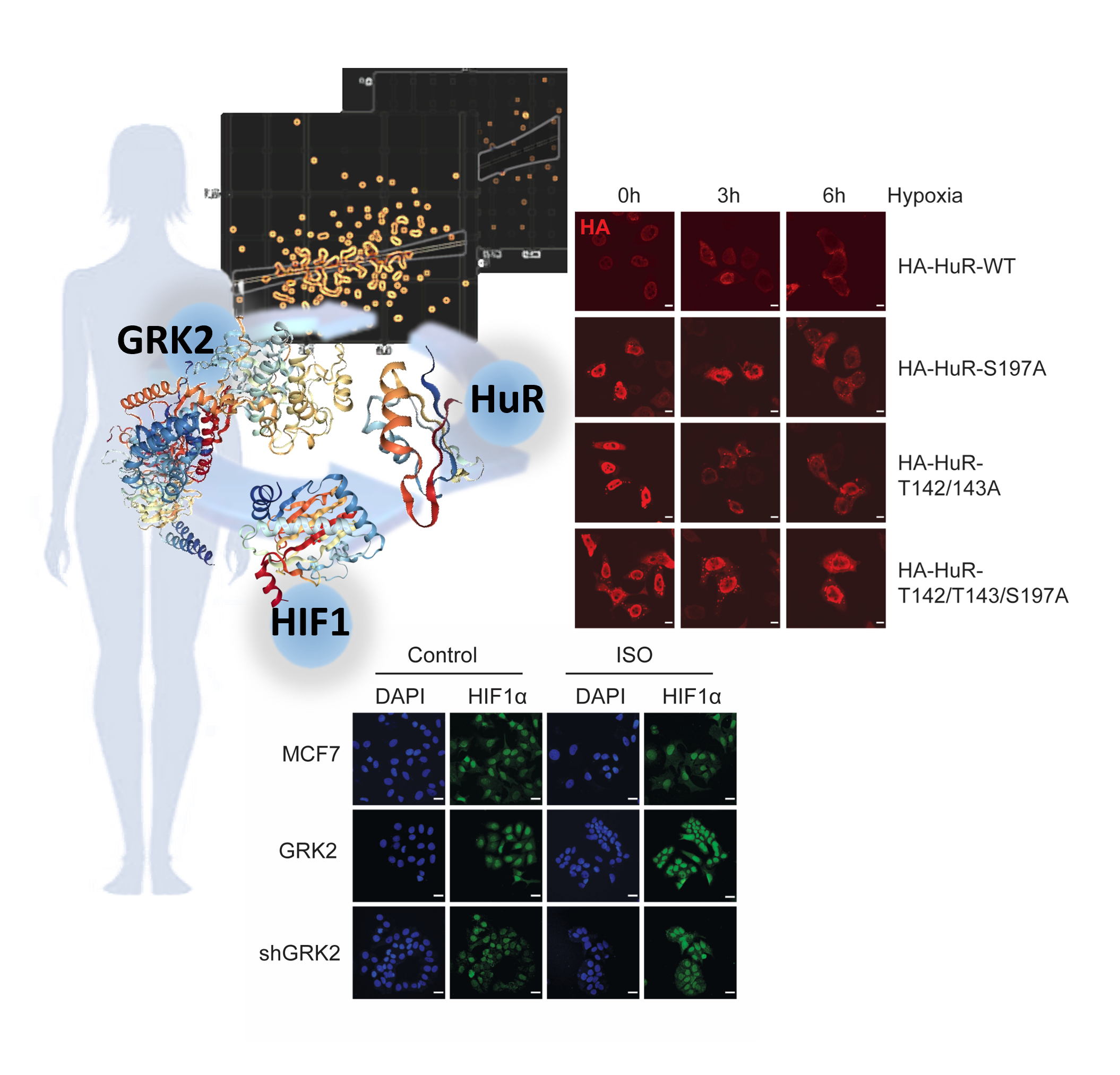
GRK2-Dependent HuR Phosphorylation Regulates HIF1α Activation under Hypoxia or Adrenergic Stress
Clara Reglero et al.
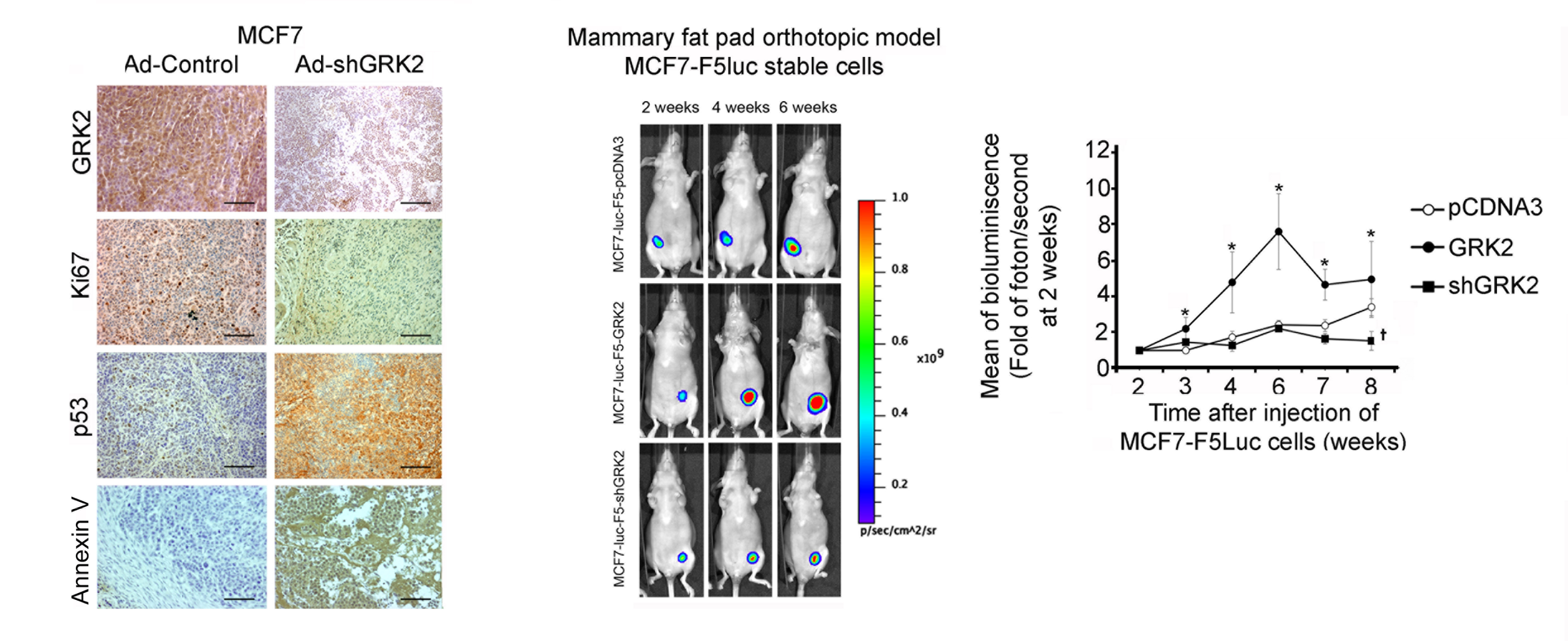
G Protein-coupled Receptor Kinase 2 (GRK2) Promotes Breast Tumorigenesis Through a HDAC6-Pin1 Axis
Laura Nogués et al.
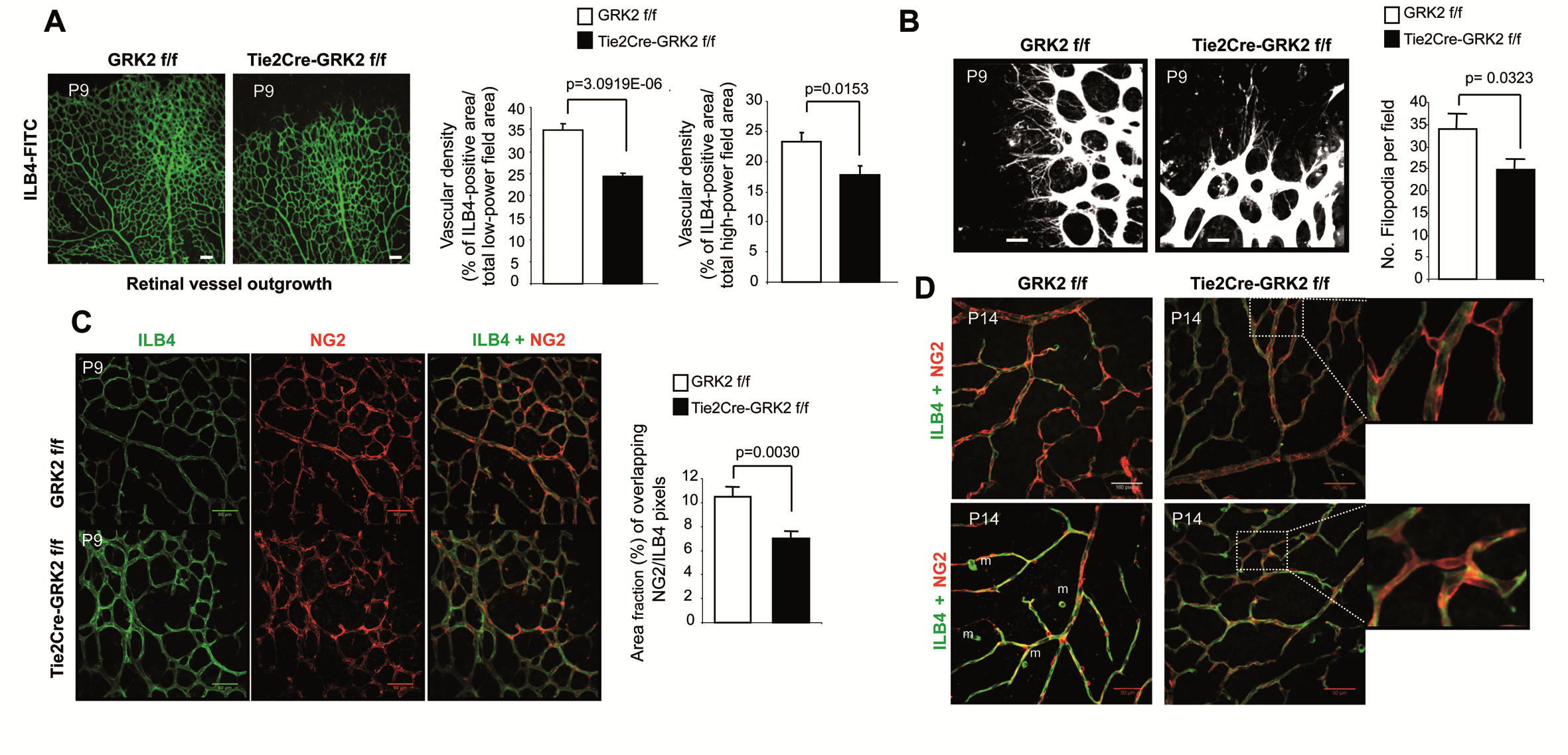
Developmental and tumoral vascularization is regulated by G protein–coupled receptor kinase 2
Verónica Rivas et al.
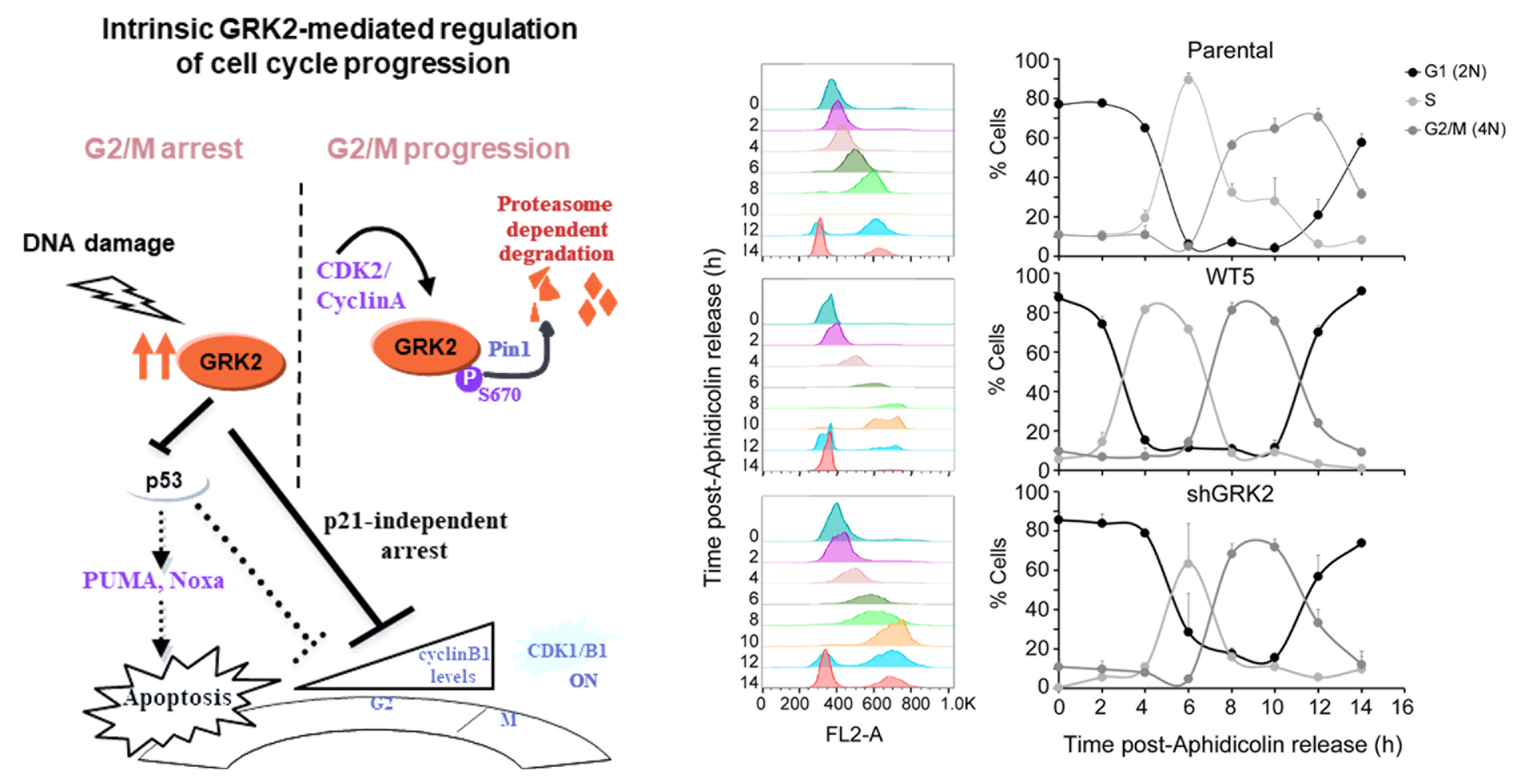
G protein–coupled receptor kinase 2 (GRK2) modulation and cell cycle progression
Petronila Penela et al.