Programa Científico
Procesos fisiológicos y patológicos
UNIDADES EN ESTE PROGRAMA
Neuropatología molecular Redes metabólicas y de señalización en la enfermedad
GRUPO DE INVESTIGACIÓN
Inflamación vascular y autofagia

Natalia Reglero Real
Nuestro laboratorio está interesado en explorar la interacción entre las células inmunitarias y el sistema vascular durante la inflamación fisiológica y patológica con el fin de identificar nuevas estrategias terapéuticas que permitan modular las enfermedades inflamatorias. Para responder a nuestras preguntas de investigación utilizamos una variedad de técnicas in vitro e in vivo, incluyendo microscopía de alta resolución, proteómica cuantitativa y modelos murinos de inflamación.
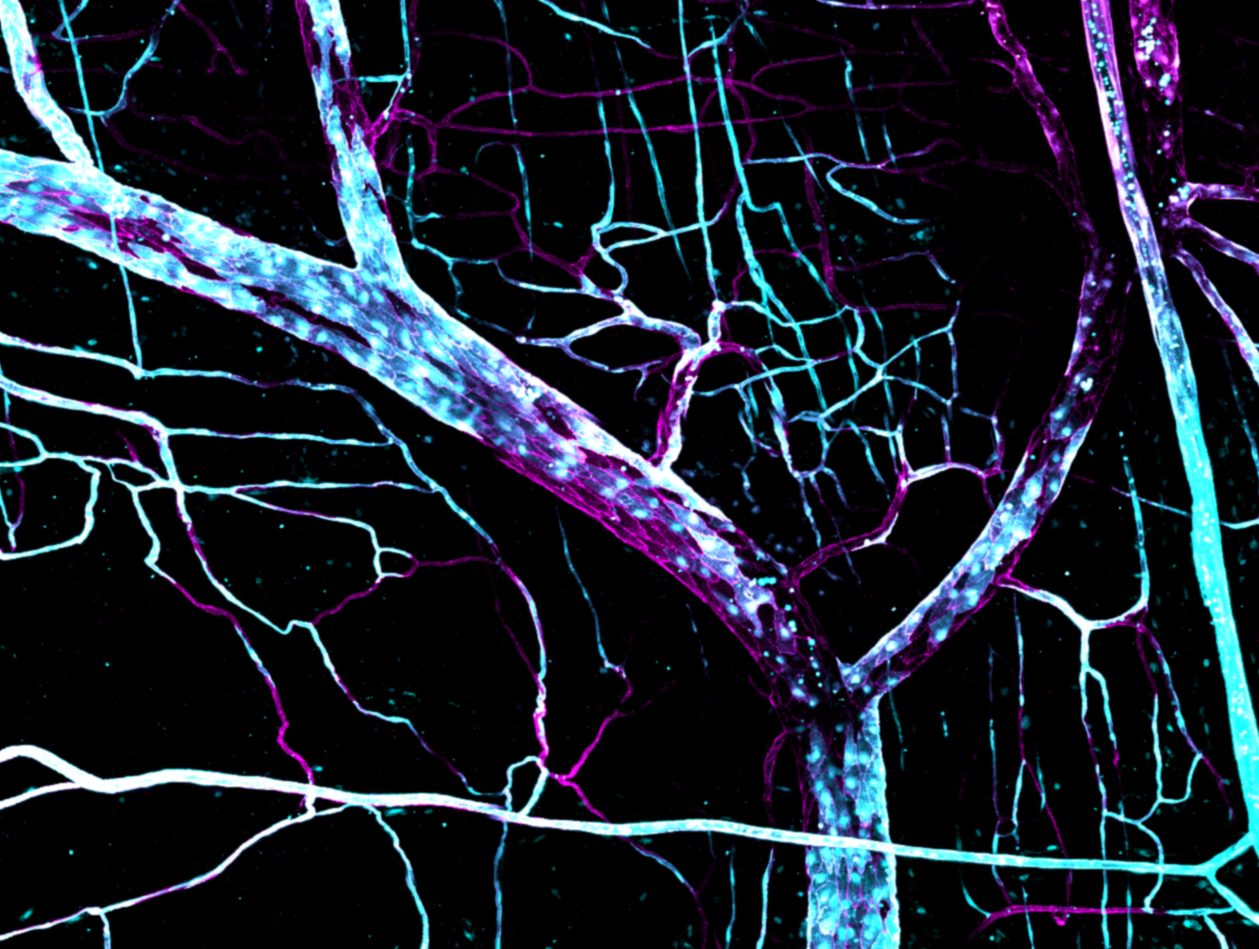
Investigación
La inflamación está en la base de una plétora de enfermedades con orígenes etiológicos muy diferentes. Aunque esta reacción inmunitaria desempeña un papel primordial durante la supervivencia del huésped y la reparación de los tejidos, la inflamación debe estar estrictamente regulada para evitar un daño excesivo de los tejidos y la instigación de enfermedades inflamatorias. Por ejemplo, la infiltración descontrolada de células inmunitarias desde los vasos sanguíneos a los tejidos lesionados, así como una permeabilidad vascular aberrante, pueden conducir al desarrollo de numerosas patologías, entre ellas afecciones cardiovasculares, metabólicas e infecciosas de gran prevalencia, así como a la progresión tumoral. Por lo tanto, comprender los mecanismos por los que la vasculatura se vuelve disfuncional durante la inflamación patológica es un área de investigación de enorme interés.
En los últimos años se ha descrito que la autofagia, un proceso metabólico, de control de la calidad del citoplasma y homeostático en general, es también clave para la correcta función del sistema inmunitario. Hasta ahora, la mayoría de esta evidencia proviene de la regulación por parte de la autofagia de la supervivencia, diferenciación, polarización y generación de mediadores inflamatorios de las propias células inmunitarias. Sin embargo, nuestro grupo ha demostrado que los procesos de autofagia de las células endoteliales, el portal que gobierna la entrada de leucocitos y macromoléculas a los tejidos, son esenciales para limitar el reclutamiento tisular de neutrófilos durante la inflamación aguda, así como el daño tisular asociado. A pesar de ello, aún se desconocen los mecanismos moleculares y la naturaleza de los procesos de autofagia que regulan este fenómeno. Por lo tanto, el principal objetivo de nuestro laboratorio emergente es descifrar los mecanismos moleculares a través de los cuales las vías de autofagia endotelial configuran la respuesta inflamatoria con el fin de identificar nuevas dianas terapéuticas para el tratamiento de enfermedades con un componente inflamatorio. En conjunto, pretendemos explorar los factores iniciadores, las características moleculares y la relevancia fisiopatológica de los procesos de autofagia endotelial durante la inflamación aguda y crónica y las patologías asociadas al envejecimiento.
Miembros del grupo

Natalia Reglero Real
Lab.: 304 Ext.: 4498
nreglero(at)cbm.csic.es

Dafne García Mateos
Lab.: 304 Ext.: 4656
dafne.garcia(at)cbm.csic.es

Guillermo Marcos Zapatero
Lab.: 304 Ext.: 4656
gmarcos(at)cbm.csic.es

Irene Carriles Moar
Lab.: 304 Ext.: 4656
irene.carriles(at)cbm.csic.es

Juan de la Cruz Fernandez
Lab.: 304 Ext.: 4498
Publicaciones representativas
Autophagy modulates endothelial junctions to restrain neutrophil diapedesis during inflammation
Natalia Reglero-Real et al.
Age-related changes in the local milieu of inflamed tissues cause aberrant neutrophil trafficking and subsequent remote organ damage
Anna Barkaway et al.
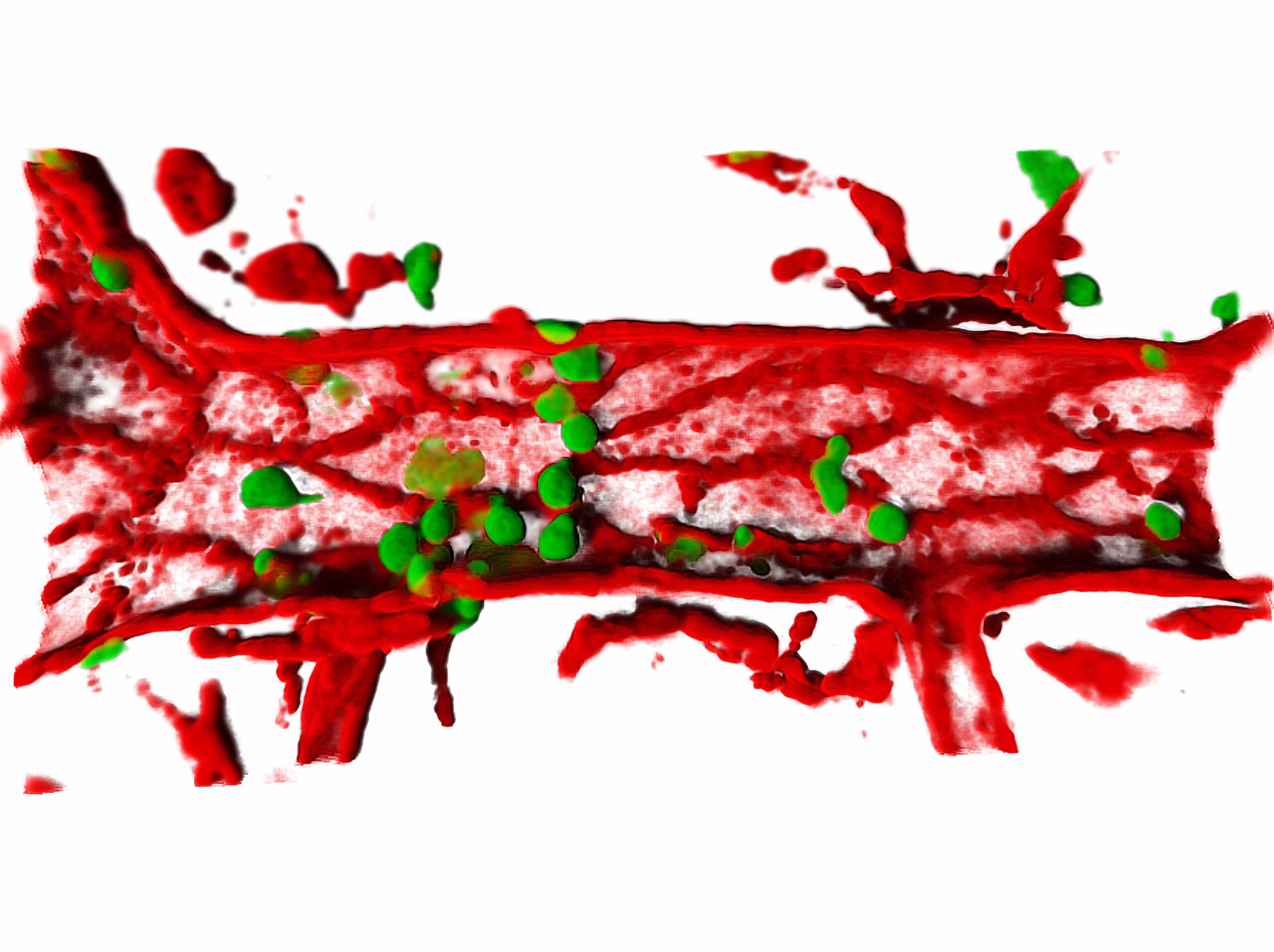
Endothelial Cell Junctional Adhesion Molecules: Role and Regulation of Expression in Inflammation
Natalia Reglero-Real et al.
Apicobasal Polarity Controls Lymphocyte Adhesion to Hepatic Epithelial Cells
Natalia Reglero-Real et al.