Servicios científicos
Citometría de flujo
Responsable del servicio

Berta Raposo
Coordinador científico

María Luisa Toribio
Contacto
91 196 44 99
citometria (at) cbm.csic.es
Sistema de reservas
Reactivos
Tarifas
En el servicio de Citometría de flujo del CBM, nuestro personal proporciona apoyo científico-técnico en citometría de flujo, desarrolla y optimiza nuevas aplicaciones y realiza separaciones celulares.
La citometría de flujo es una herramienta analítica que permite discriminar partículas de diferente tamaño y color. Es una técnica analítica y/o preparativa basada en el análisis simultáneo de varios parámetros de naturaleza óptica, de forma rápida y sobre un gran número de partículas individualizadas. Este análisis se realiza sobre cada partícula a partir de la dispersión de la luz y de la emisión de fluorescencia de las partículas iluminadas por una fuente luminosa.
Los parámetros que pueden analizarse mediante citometría de flujo son: i) los relacionados con las características físicas de la partícula: tamaño y complejidad y ii) las diferentes fluorescencias asociadas a la partícula.
El análisis se realiza a tasas de miles de células/segundo, lo que permite obtener datos de gran fiabilidad estadística, así como identificar poblaciones representadas a baja frecuencia dentro de la población global.
Otra característica importante de la citometría de flujo es que el análisis se realiza en una suspensión de partículas, por lo que las partículas o células analizadas deben estar en suspensión y en forma de partícula única (célula).
Por último, es importante señalar que existe una restricción en cuanto al tamaño de las partículas analizadas, que debe estar comprendido entre 0,5 y 100um.
Vacío
Citometría convencional
|
FACSCalibur (Becton Dickinson)
Software de adquisición: Cell Quest-Pro |
 |
|
FACSCanto A (Becton Dickinson)
Software de adquisición: DiVA 8.0.1 |
 |
|
FACSCanto II HTS (Becton Dickinson) Características técnicas:
4 detectores para el láser de 488 nm (azul): 530/30, 585/42, 695/40, 780/60 Software de adquisición: DiVA 8.0.1 |
 |
|
FACSCanto II High (sólo tubos) (Becton Dickinson) Software de adquisición: DiVA 8.0.1 |
 |
Citometría espectral
| AURORA 4L (Cytek) Configuración óptica: 4L (16V-14B-10YG-8R) 4 líneas láser y 48 detectores: 16 detectores para el láser violeta (405nm), 14 detectores para el azul (488nm), 10 detectores para el verde amarillo (561nm) y 8 detectores para el rojo (633nm). Características técnicas: Este equipo utiliza tecnología de espectro completo proporcionando una gran flexibilidad a los usuarios, permitiéndoles el uso de una amplia gama de fluorocromos combinándolos mucho más fácilmente que con otras tecnologías. Además, mejora la resolución de las poblaciones especialmente en muestras con alta autofluorescencia y/o bajos niveles de expresión de marcadores. Este equipo está dotado además con un módulo de alta sensibilidad en el detector de SSC que permite resolver partículas de menor tamaño que otros equipos logrando separarlas más fácilmente del ruido electrónico. (ESP, Enhanced Small Particle Detector) |
| AURORA 5L ESP (Cytek) Configuración óptica: 5L (16UV-16V-14B-10YG-8R) 4 líneas láser y 64 detectores: 16 detectores para el láser ultravioleta (355nm),16 detectores para el láser violeta (405nm), 14 detectores para el azul (488nm), 10 detectores para el verde amarillo (561nm) y 8 detectores para el rojo (633nm). Características técnicas: Este equipo utiliza tecnología de espectro completo proporcionando una gran flexibilidad a los usuarios, permitiéndoles el uso de una amplia gama de fluorocromos combinándolos mucho más fácilmente que con otras tecnologías. Además, mejora la resolución de las poblaciones especialmente en muestras con alta autofluorescencia y/o bajos niveles de expresión de marcadores. Este equipo está dotado además con un módulo de alta sensibilidad en el detector de SSC que permite resolver partículas de menor tamaño que otros equipos logrando separarlas más fácilmente del ruido electrónico. (ESP, Enhanced Small Particle Detector) |
Cell sorters
| FACSAria Fusion (Becton Dickinson) El BD FACSAria Fusion es un separador celular fácil de usar que permite la separación de un gran número de muestras de diferentes orígenes. Se instala en una cabina de bioseguridad de Clase II Tipo A2 equipada con un sistema integrado de contención de aerosoles que funciona de forma independiente. A continuación se detallan algunas características técnicas: Equipada con cuatro láseres de excitación de 405, 488, 561 y 640 nm. 18 detectores (16 de fluorescencia + 2 de dispersión), de los cuales 5 son para el láser de 405 nm (450/40, 525/50, 610/20, 660/20, 710/50, 780/60) y 2 para el láser de 488 nm: 530/30, 695/20, 4 para el láser de 561 nm: 610/20, 670/14, 710/50, 780/60 y 3 para el láser de 640 nm: 670/30, 730/45, 780/60. También está equipado con un sistema de control de temperatura y agitación de muestras. |
 |
Estaciones de análisis y software
El servicio pone a disposición de los usuarios tres estaciones de análisis (Hewlett-Packard) equipadas con los siguientes programas para analizar datos de citometría e imagenes:
– Estación 1: FlowJo v10 y 7.6.5, Spectroflo3.3.1 (configuración de 4 o 5 L)
– Estación 2: FlowJo v10, Spectroflo 3.3. 1 (configuración de 4 L)
– Estación 3: FlowJo v10, Spectroflo 3.3.1 (configuración de 5 L), Gen5 y DIVA 9.
Además, el servicio pone a disposición de los usuarios una licencia del software on line OMIQ (una moderna plataforma de análisis de citometría de flujo basada en el uso de algoritmos matemáticos automatizados a la vez que permiten análisis clásico de gating manual.
Otros equipos
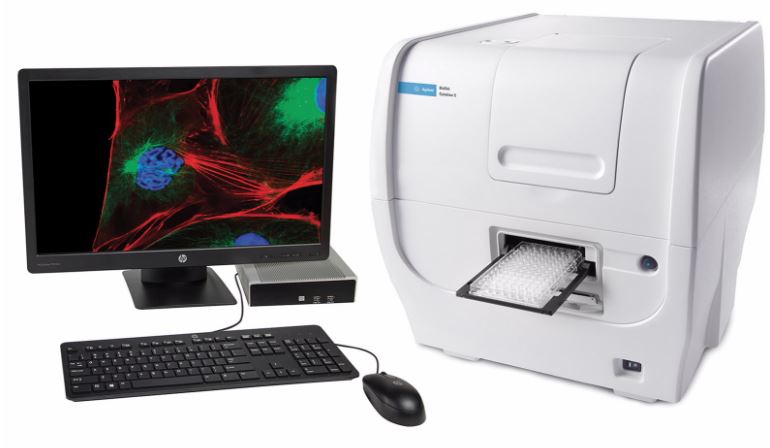
| Cytation (Agilent) Características técnicas: El citómetro multimodal Cytation 1 de BioTek combina imágenes de fluorescencia y campo claro de alto contraste con la detección multimodal convencional. Este microscopio está equipado con un objetivo 4X y 3 líneas de fluorescencia: – DAPI (EX 377/50 nm, EM 447/60 nm); LED 365 nm. – GFP (EX 469/35 nm, EM 525/39 nm); LED 465 nm – RFP (EX 531/40 nm, EM 593/40 nm); LED 523 nm El software de adquisición Gen5 simplifica la captura de imágenes y la lectura de placas. |
 |
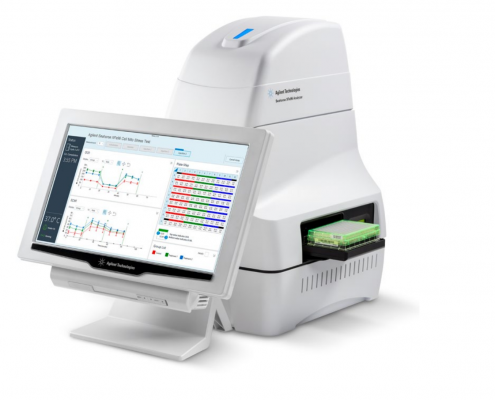
| eFlux Analyzer XF96 (Agilent) Características técnicas: El analizador de flujo extracelular XF96 (Agilent-Seahorse) permite caracterizar el metabolismo energético de células cultivadas de forma no invasiva. El instrumento analiza el consumo de oxígeno (OCR) y la acidificación extracelular (ECAR, una medida indirecta de la producción de lactato) en placas de 96 pocillos. Nuestro servicio proporciona acceso al equipo, así como asistencia básica tanto en el diseño de experimentos como en el análisis de datos. |
 |
|
NanoSight NS300 (Malvern Panalytical) Aplicaciones: |
 |
Información adicional
- PRESTACIONES
Las prestaciones ofertadas se encuentran publicadas en el catálogo de prestaciones del CSIC y son anualmente actualizadas y revisadas. Para la presente campaña se ofertan las siguientes prestaciones con sus respectivas variantes:
- Adquisición de en citómetros analíticos
- Citometría analítica convencional 2 láseres CON O SIN ASISTENCIA*
- Citometría analítica convencional 3 láseres CON O SIN ASISTENCIA*
- Citometría analítica espectral 4 láseres CON O SIN ASISTENCIA*
- Citometría analítica espectral 5 láseres CON O SIN ASISTENCIA*
* se requiere formación previa
- Clasificación celular**
** siempre uso con asistencia
- Análisis de datos
- Suministro de reactivos
- TIPOS DE TÉCNICAS UTILIZADAS
Algunos de los protocolos técnicos realizados en nuestro servicio incluyen:
- Inmunofenotipaje (con anticuerpos específicos y diversos fluorocromos)
- Viabilidad celular (DAPI, ioduro de Propidio)
- Análisis del ciclo celular y de la ploidía
- Análisis de la expresión génica mediante genes reporteros (GFP, CFP, dsRed, mCherry, BFP…)
- Medida de la división celular y proliferación (CFSE, Cell Trace Violet)
- Análisis de proliferación mediante BrdU o tecnología Click-iT ™EdU
- Inducción de apoptosis (Anexina V, Caspasa 3, TUNEL)
- Flujo de calcio (Fluo 3/Fura Red, INDO 1)
- Señalización intracelular: detección de fosfoproteínas y proteínas citosólicas a nivel unicelular
- Ensayos Multiplexados de moléculas en disolución (citoquinas, fosfoproteínas)
- Análisis de los niveles de especies derivadas del O2
- Análisis del potencial de membrana
- Contaje celular absoluto
- Análisis de fagocitosis
- Caracterización del metabolismo energético celular por consumo de oxígeno (OCR) y acidificación extracelular (ECAR, una medida indirecta de la producción de lactato) en placas de 96 pocillos.
- Determinaciones de interacciones proteína-proteína basadas en FRET.
- Análisis de función metabólica celular
- Separaciones celulares a alta velocidad en base a parámetros fluorescentes…
CUALQUIER OTRA TÉCNICA O PROTOCOLO QUE NO APAREZCA EN LA LISTA ES SUSCEPTIBLE DE IMPLEMENTARSE BAJO DEMANDA
- MUESTRAS ANALIZADAS
El servicio admite una amplia variedad de muestras biológicas, entre las que se incluyen:
- Líneas celulares de mamífero (humanas, ratón, perro, hámster…)
- Exosomas y microvesículas producidas in vitro por células en cultivo
- Sobrenadantes celulares y sueros de ratón
- Células primarias fundamentalmente de ratón, pero también de Drosophila, Zebrafish y humanas
- Protoplastos vegetales
- Núcleos aislados tanto de células de mamífero como vegetales
- Bacterias y levaduras
CUALQUIER OTRA MUESTRA COMPATIBLE CON LA TÉCNICA QUE NO APAREZCA EN LA LISTA ES SUSCEPTIBLE DE IMPLEMENTARSE BAJO DEMANDA
- PERSONAL
| NOMBRE Y APELLIDOS | PUESTO |
| Raquel Nieto Pintado | Técnico senior |
| Silvia Andrade Calvo | Técnico senior |
| Matilde Riquelme Sánchez | Técnico |
| Berta Raposo Ponce | Responsable de servicio |
| Maria Luisa Toribio | Responsable científico |
Personal

Berta Raposo Ponce
Lab.: 111 Ext.: 4499
braposo(at)cbm.csic.es

Raquel Nieto Pintado
Lab.: 111 Ext.: 4698/4705
rnieto(at)cbm.csic.es

Silvia Andrade Calvo
Lab.: 111 Ext.: 4698/4705
sandrade(at)cbm.csic.es

Matilde Riquelme Sánchez
Lab.: 111 Ext.: 4698/4705
mriquelme(at)cbm.csic.es

