Un equipo multidisciplinar del Centro de Biología Molecular Severo Ochoa (CBM, CSIC-UAM), el Instituto de Química Física Blas Cabrera (CSIC) y el Instituto de Catálisis y Petroleoquímica (CSIC), ha identificado y caracterizado en detalle una nueva enzima con un gran potencial para mejorar la producción de prebióticos, compuestos cada vez más importantes en alimentación y salud.
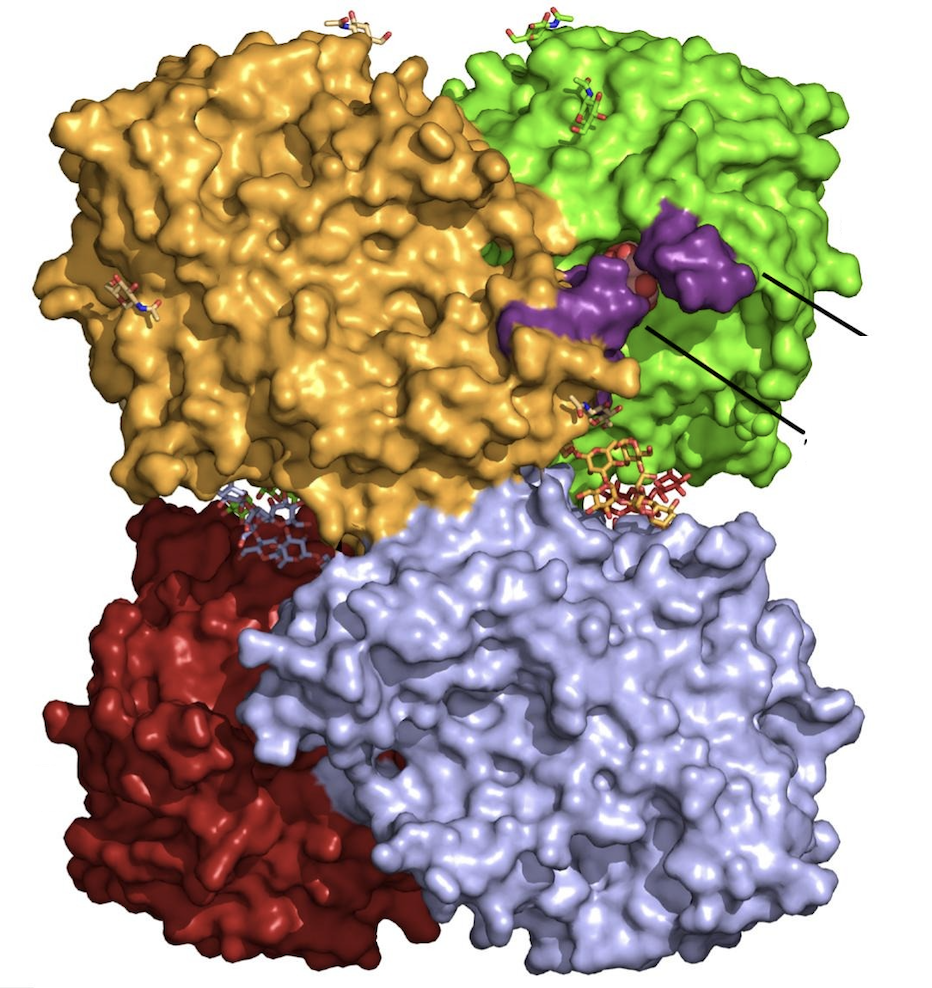
El trabajo, publicado en la revista científica International Journal of Biological Macromolecules, describe por primera vez la estructura tridimensional y el mecanismo de acción de una enzima llamada β-fructofuranosidasa, procedente del hongo Purpureocillium lilacinum. Esta proteína es capaz de transformar azúcares simples en moléculas más complejas con propiedades beneficiosas para nuestro organismo.
¿Qué son los prebióticos y por qué son importantes?
Los prebióticos son tipos especiales de azúcares que nuestro cuerpo no puede digerir, pero que sirven de alimento para las bacterias “buenas” que viven en el intestino. Entre los más conocidos están los fructooligosacáridos (FOS), presentes de forma natural en alimentos como la cebolla o el plátano.
Consumir estos compuestos ayuda a mantener una microbiota intestinal equilibrada, lo que se relaciona con mejoras en la digestión, el sistema inmunitario e incluso el bienestar general. Por eso, la industria alimentaria está muy interesada en producir FOS de manera controlada y eficiente. Ahí es donde entran en juego enzimas como la estudiada en este trabajo.
Las β-fructofuranosidasas son proteínas capaces de cortar y unir moléculas de azúcar. Dependiendo de cómo funcionen, pueden simplemente descomponer la sacarosa (el azúcar común) o transformarla en oligosacáridos más complejos y valiosos.
La enzima analizada en este estudio, bautizada como PlINV, ha demostrado ser especialmente interesante porque tiene una gran capacidad para generar distintos tipos de FOS. Además, los investigadores han descubierto que posee una organización estructural completamente nueva dentro de su familia de enzimas.
“Gracias a las técnicas de cristalografía hemos podido ver, átomo a átomo, cómo está organizada esta proteína y cómo interacciona con los azúcares”, explica María Fernández Lobato, investigadora del CBM y una de las responsables del trabajo. “Conocer su estructura es fundamental para entender cómo funciona y cómo podemos mejorarla”.
Diseñar enzimas a medida
El estudio combina el análisis estructural con técnicas de ingeniería genética: el equipo modificó determinados aminoácidos de la enzima para comprobar cómo cambiaba su actividad.
El resultado fue muy prometedor: algunas variantes produjeron más cantidad de prebióticos y otras generaron tipos concretos de azúcares con mayor selectividad.
“Demostramos que es posible ajustar el comportamiento de la enzima como si fuera una herramienta programable”, señala Eglė Narmontaitė, investigadora del CBM y primera autora del artículo. “Esto nos permite imaginar biocatalizadores diseñados específicamente para cada aplicación industrial”.
Más allá de los alimentos
La utilidad de esta enzima no se limita solo a la producción de prebióticos. El estudio también ha mostrado que PlINV es capaz de modificar otras moléculas de interés, como compuestos polifenólicos con propiedades antioxidantes.
Este tipo de reacciones abre nuevas posibilidades para crear ingredientes funcionales, nutracéuticos (alimento con beneficio específico para la salud) o incluso productos con aplicaciones farmacéuticas.
El uso de enzimas como herramientas biotecnológicas ofrece una alternativa más limpia y sostenible frente a los procesos químicos tradicionales. Permiten fabricar compuestos de alto valor añadido con menos residuos y menor consumo energético.
Según Fernández Lobato, “este trabajo es un ejemplo claro de cómo la investigación básica, centrada en entender a fondo cómo funcionan las proteínas, puede transformarse en aplicaciones reales con impacto directo en la sociedad”.
El descubrimiento de esta nueva enzima y la comprensión detallada de su funcionamiento representan un paso importante hacia el desarrollo de procesos industriales más eficientes y saludables, basados en la enorme capacidad de los microorganismos para generar moléculas beneficiosas.
Referencia
Narmontaite, E., Ruiz-Núñez, M., Plou, F.J., Fernández-Lobato, M., Sanz-Aparicio, J. Structural and mechanistic insights into a novel β-fructofuranosidase from Purpureocillium lilacinum with high transfructosylating activity and an atypical tetrameric assembly. International Journal of Biological Macromolecules (2026).