Bases moleculares de la patogénesis vascular y de la linfomagénesis
Resumen de Investigación:
El objetivo de nuestro grupo es descubrir nuevas dianas terapéuticas para las dos principales causas de mortalidad en el Mundo: el cáncer y las enfermedades cardiovasculares. Nuestra investigación se centra en identificar los mecanismos moleculares alterados en estas enfermedades empleando una combinación de abordajes experimentales in vitro e in vivo que incluye análisis transcriptómicos, proteómicos, celulares y moleculares; generación de modelos animales de las patologías y técnicas avanzadas de imagen.
BASES MOLECULARES DE LA PATOGÉNESIS VASCULAR
Nuestros estudios pioneros, en colaboración con el grupo del Dr. J.M. Redondo (CNIC), han mostrado que la deficiencia de la metaloproteasa Adamts1 provoca la formación de aneurismas de la aorta torácica (AAT) en ratones debido a la inducción de Nos2, la sintasa inducible de óxido nítrico (NO), y el consecuente aumento de la producción de NO. También hemos mostrado que la inhibición farmacológica de Nos2 revierte la formación de AAT en modelos múridos, sugiriendo la posibilidad de que el bloqueo de la ruta de señalización del NO podría constituir un tratamiento eficaz para el AAT. De hecho, estamos preparando la realización de un ensayo clínico con inhibidores de NOS2 en pacientes de síndrome de Marfan, una enfermedad genética en la que el AAT es responsable de más del 90% de su letalidad. Estos descubrimientos han cambiado nuestra visión de la fisiopatología del AAT y nos han llevado a continuar investigando los mecanismos moleculares y biomecánicos en colaboración con grupos de investigación de otros países. Buena parte de nuestro trabajo actual se centra en la identificación de mediadores adicionales de estas enfermedades.
También estamos interesados en descubrir genes capaces de mediar el remodelado patológico de la pared de los vasos, un proceso crítico en el desarrollo de la hipertensión arterial y de enfermedades como la aterosclerosis y los aneurismas de la aorta ascendente y de la aorta abdominal (AAA). Hace pocos años determinamos que la calcineurina y Rcan1, uno de los genes inducidos en la aorta tras su activación, son mediadores esenciales de la aterosclerosis, la restenosis y los AAA. Los resultados de nuestra investigación permitieron identificar nuevos mecanismos fisiopatológicos y nuevas dianas terapéuticas para las enfermedades aórticas. Empleando ratones en los que podíamos inducir la deleción de Rcan1 en tipos celulares determinados descubrimos que Rcan1 desempeña un papel homeostático en la aorta y que su inactivación genética en ratones adultos predispone a la formación de hematomas intramurales y, posteriormente, AAA en respuesta a la hipertensión arterial. Demostramos, además, que proteínas como GSK-3beta, ROCK y la Miosina específica de músculo liso juegan un papel crítico en estos procesos. Estos resultados nos han llevado a abrir nuevas y excitantes líneas de investigación de la patogénesis de las enfermedades aórticas. En particular, recientemente hemos iniciado un exhaustivo estudio encaminado a determinar el papel de la calcineurina en la regulación de los cambios en el transcriptoma, el proteoma y el fosfoproteoma de la aorta inducidos por estímulos hipertensivos como la angiotensina II. Creemos que esta investigación nos permitirá identificar dianas terapéuticas adicionales para el tratamiento de la hipertensión arterial y de los aneurismas aórticos.
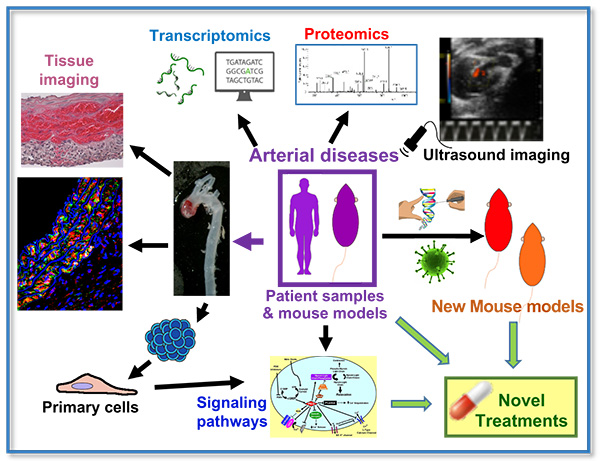
Figura 1: El empleo de transcriptómica, proteómica, análisis de tejidos y cultivos primarios de modelos múridos y/o de muestras derivadas de pacientes nos permite diseccionar las principales rutas de señalización causantes de enfermedades de las arterias, como los aneurismas aórticos y la hipertensión arterial, e identificar dianas para la intervención terapéutica. Mediante la manipulación genética o la transducción in vivo con lentivirus generamos nuevos modelos múridos para la validación de estas dianas. Comprobamos la eficacia de nuevos tratamientos mediante el análisis longitudinal de imágenes de ecografía de corazón y vasos in vivo y de imágenes de tejidos ex vivo.
BASES MOLECULARES DE LA LINFOMAGÉNESIS
La inmortalización celular es un paso necesario, pero no suficiente, para la transformación tumoral. Las Líneas Celulares Linfoblastoides (LCLs), producidas por infección de linfocitos B normales de donantes sanos con el virus de Epstein-Barr, son ejemplos de células inmortales, pero no tumorales. Al contrario que las células de linfoma (tumorales), las LCLs y los linfocitos primarios normales no forman tumores tras su inoculación en ratones inmunodeficientes y no crecen en medios semisólidos como el agar blando. El crecimiento en geles blandos es característico, en particular, de las Células Iniciadoras de Tumores (CITs), las cuales son especialmente resistentes a la mayoría de las terapias actuales y causantes de las recidivas. Uno de nuestros objetivos principales es descubrir dianas terapéuticas en las células iniciadoras de tumores. Para ello estamos empleando diversos abordajes experimentales, incluyendo la comparación de la expresión génica de LCLs con la de linfocitos B tumorales (linfomas y leucemias). Hemos identificado más de 1600 genes expresados diferencialmente entre células de linfoma y LCLs y hemos iniciado el estudio de varios candidatos. Hemos descubierto que la expresión de uno de ellos, CDCA7, se encuentra anormalmente elevada en todas las líneas celulares de tumores linfoides analizadas y en biopsias de linfomas derivadas de pacientes; que su expresión elevada en linfomas/leucemias es necesaria para su crecimiento en medios semisólidos y para la formación de tumores en ratones inmunodeficientes, pero no es requerida para la proliferación celular en medio líquido, y que también es necesaria para la migración e invasividad de los linfomas mediante su capacidad para regular la dinámica de los citoesqueletos de tubulina y de actomiosina. Con financiación de la Fundación de la Asociación Española Contra el Cáncer estamos investigando los mecanismos implicados en el crecimiento diferencial en geles blandos y, además, mediante un screening de shRNAs de genoma completo nos proponemos identificar genes adicionales requeridos para el crecimiento en estos geles. Determinaremos posteriormente la contribución de algunos de estos genes al crecimiento de varios tipos de leucemias y linfomas en geles blandos y emplearemos herramientas genéticas para bloquear su expresión y drogas que inhiban su actividad para determinar su potencial terapéutico en modelos animales. Confiamos en que este trabajo nos permitirá identificar proteínas necesarias para la proliferación de las CITs y fármacos que las modulen, lo que facilitará el desarrollo de terapias para el tratamiento de los linfomas y las leucemias más específicas, con menos efectos secundarios y menos propensas a la recaída que las actuales.
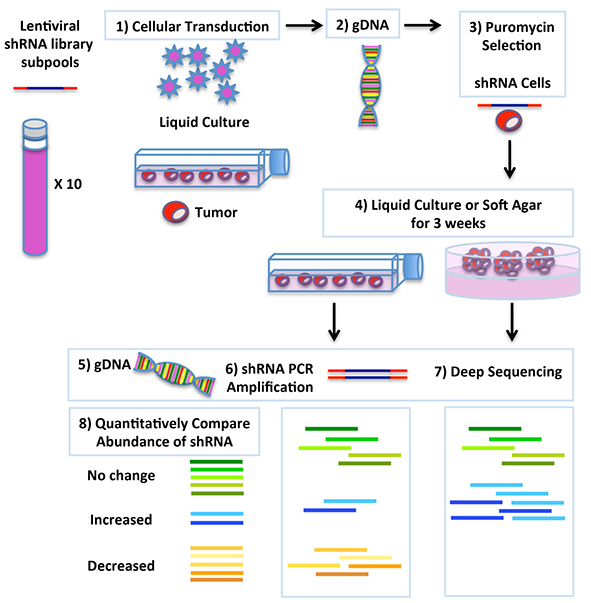
Figura 2: Esquema del diseño experimental de escrutinio de una genoteca de shRNAs del genoma completo empleado para el descubrimiento de genes implicados en el crecimiento de las células iniciadoras de tumores.

| Apellidos | Nombre | Laboratorio | Ext.* | Categoría profesional | |
|---|---|---|---|---|---|
| Campanero García | Miguel R. | 227 | 4554 | mcampanero(at)cbm.csic.es | E. Investigadores Científicos de Organismos Públicos |
| Clemente Toribio | Cristina | 227 | 4587 | cristina.clemente(at)cbm.csic.es | Titulado Superior Grado de Doctor |
| Gil Ruiz | Teresa | 227 | 4587 | Becario JAE Intro | |
| Gutiérrez Martínez | Carolina | 227 | 4587 | carolina.gutierrez(at)cbm.csic.es | Titulado Sup. Actividades Tecn. y Prof.GP1 |
| Hernández Alcántara | Alberto | 227 | 4587 | ahernandez(at)cbm.csic.es | M2 |
| Redondo Moya | Juan Miguel | 227 | 4401 | jmredondo(at)cbm.csic.es | E. Profesores de Investigación de Organismos Públicos de Investigación |
| Reyes Campos | Oliva | 227 | 4554 | Estudiante | |
| Sun | Yilin | 227 | 4587 | yilin.sun(at)cbm.csic.es | M2 |
Publicaciones relevantes:
- de la Fuente-Alonso, M. Toral, A. Alfayate, M.J. Ruiz-Rodríguez, E. Bonzón-Kulichenko, G. Teixido-Tura, M.J. Méndez-Olivares, D. López-Maderuelo, I. González-Valdés, E. García-Izquierdo, S. Mingo, C.E. Martín, L. Muiño-Mosquera, J. De Backer, J.F. Nistal, A. Forteza, A. Evangelista, J. Vázquez, *M.R. Campanero, and *JM Redondo. *Co-senior & corresponding authors. Aortic disease in Marfan syndrome is caused by overactivation of sGC-PRKG signaling by NO. Nat. Commun. (2021) 12(1): 2628.
- Toral, A. de la Fuente-Alonso, *M.R. Campanero, and *J.M. Redondo. *Co-senior & corresponding authors. The Nitric Oxide Signalling Pathway in Aortic Aneurysm and Dissection. Brit. J. Pharmacol. (2021) doi: 10.1111/bph.15694.
- Martín-Cortázar, Y. Chiodo, R. Jiménez-P., M. Bernbé, M.L. Cayuela, T. Iglesias, and M.R. Campanero. CDCA7 finely tunes cytoskeleton dynamics to promote lymphoma migration and invasion. Haematologica. (2020) 105(3): 730-740.
- S Villahoz, PS Yunes-Leites, N Méndez-Barbero, K Urso, E.Bonzon-Kulichenko, S Ortega, J Vazquez, S Offermanns, *JM Redondo, and *MR Campanero. *Co-senior & corresponding authors. Conditional deletion of Rcan1 predisposes to hypertension-mediated aortic intramural hematoma and subsequent aneurysm and lethal dissection. Nat Commun (2018) 9(1): 4795.
- Jiménez-P., C. Martín-Cortázar, O. Kourani, Y. Chiodo, R. Cordoba, M.P. Domínguez-Franjo, J.M. Redondo, T. Iglesias, and M.R. Campanero. CDCA7 is a critical mediator of lymphomagenesis that selectively regulates anchorage-independent growth. Haematologica. (2018) 103(10): 1669-1678.
- Oller, N. Méndez-Barbero, E.J. Ruiz, S. Villahoz, M. Renard, L.I. Canelas, A.M. Briones, R. Alberca, N. Lozano-Vidal, M.A. Hurlé, D. Milewicz, A. Evangelista, M. Salaices, J.F. Nistal, L.J. Jiménez-Borreguero, J. DeBacker, *M.R. Campanero, and *J.M. Redondo. *Co-senior & corresponding authors. Nitric oxide mediates aortic disease in mice deficient in the metalloprotease Adamts1 and in a mouse model of Marfan syndrome. Nat. Med. (2017) 23(2): 200-212 Destacado por Science: http://science.sciencemag.org/content/355/6324/twil; Destacado por Biocentury: Inducible nitric oxide synthase 2 (NOS2; iNOS).
- Alvaro-Blanco, Y. Chiodo, K. Urso, C. Martín-Cortázar, O. Kourani, M. Rodriguez-Martinez, E. Calonge, J. Alcamí, J.M. Redondo, T. Iglesias, and M.R. Campanero. MAZ induces MYB expression during the exit from quiescence via de E2F site in the MYB promoter. Nucleic Acids Res. (2017) 45(17): 9960-9975.
- Méndez-Barbero, V. Esteban, S. Villahoz, A. Escolano, K. Urso, A. Alfranca, C. Rodríguez, S.A. Sánchez, T. Osawa, V. Andrés, J. Martínez-González, T. Minami, *J.M. Redondo, and *M.R. Campanero *Co-senior & corresponding authors. A major role for RCAN1 in atherosclerosis progression. EMBO Mol. Med. (2013) 5:1901-1917.
- Molina-Privado, R. Jiménez-P., S. Montes-Moreno, Y. Chiodo, M. Rodríguez-Martínez, L. Sánchez-Verde, T. Iglesias, M.A. Piris, and R. Campanero. E2F4 plays a key role in Burkitt lymphoma tumorigenesis. Leukemia. (2012) 26(10): 2277-2285.
- V Esteban, N Méndez-Barbero, LJ Jiménez-Borreguero, M Roqué, L Novensá, AB García-Redondo, M Salaices, L Vila, ML. Arbonés, *R. Campanero, and *JM Redondo. *Co-senior & corresponding authors. Regulator of calcineurin 1 mediates pathological vascular wall remodeling. J. Exp. Med. (2011) 208: 2125-2139. Seleccionado por Faculty of 1000 (Muller W: 2012. F1000.com/13418975)
Tesis doctorales:
- Irene Molina Privado (2009). Estudio de las bases moleculares de la formación del Linfoma de Burkitt para la identificación de posibles marcadores diagnósticos y dianas terapéuticas. Universidad Autónoma de Madrid. Director: Miguel R. Campanero
- Lorena Martínez Gac (2009). Estudio de los mecanismos implicados en la regulación transcripcional de los genes CCNG2 Y C-MYC. Universidad Autónoma de Madrid. Directores: Miguel R. Campanero y Ana Clara Carrera.
- Raúl Jiménez Pérez (2013). Identificación y caracterización funcional de genes implicados en la transformación maligna del compartimento linfocitario. Universidad Autónoma de Madrid. Director: Miguel R. Campanero.
- Nerea Méndez Barbero (2014). Estudio del papel de calcineurina y Rcan1 en el remodelado patológico de la pared vascular. Universidad Autónoma de Madrid. Directores: Miguel R. Campanero y Juan Miguel Redondo.
- Yuri Chiodo (2017). Cell death, cell growth and cell cycle regulation by the Retinoblastoma family. Universidad Autónoma de Madrid. Directores: Miguel R. Campanero y Juan Miguel Redondo.
- Jorge Oller Pedrosa (2017). Identification of the metalloproteinase Adamts1 and Nitric Oxide as new therapeutic targets in aortic diseases. Universidad Autónoma de Madrid. Directores: Miguel R. Campanero y Juan Miguel Redondo.
- Silvia Villahoz Lázaro (2018). Effects of conditional deficiency of Rcan1 in pathological vascular wall remodeling (Tesis Europea). Universidad Autónoma de Madrid. Directores: Miguel R. Campanero y Juan Miguel Redondo.
- Carla Martín Cortázar (2019). Invasión, migración y dinámica del citoesqueleto de células de linfoma mediadas por CDCA7. Universidad Autónoma de Madrid. Director: Miguel R. Campanero.
- Omar Kourani Méndez (2019). Papel del sistema del glutatión en la adaptación y resistencia de los tumores linfoides al estrés oxidativo. Universidad Autónoma de Madrid. Director: Miguel R. Campanero.
Patentes licenciadas:
- Procedimiento de identificación de pacientes con linfoma de Burkitt esporádico, procedimiento de identificación y uso de compuestos para el tratamiento de linfoma de Burkitt esporádico. I. Molina-Privado y Miguel R. Campanero. PCT/ES2008/070182. País de prioridad: Internacional salvo USA. Fecha: octubre de 2007. Entidad titular: CSIC/UAM; Licenciada a BIOTOOLS Biotechnological & Medical Laboratories S.A. el 29 de abril de 2008.
- In vitro method for identifying thoracic aortic aneurysms (TAA) in a subject. J.M. Redondo, J. Oller, N. Méndez-Barbero y Miguel R. Campanero. PCT/EP2016/082925. País de prioridad: Internacional excepto USA. Fecha de prioridad: marzo de 2016; Entidad titular: CNIC/CSIC/UAM. Licenciada a SPHERIUM BIOMED S.L. el 21 de septiembre de 2018. Patente USA (Nº 16/083,165) concedida el 16 de septiembre de 2020.




















