Autofagia no convencional y sus implicaciones en fisiología y patología
Resumen de Investigación:
La autofagia es un proceso degradativo que elimina componentes celulares prescindibles o potencialmente dañinos y es crítico para el mantenimiento de la homeostasis celular. A juzgar por los fenotipos patológicos que se observan en ratones deficientes en las proteínas que constituyen la maquinaria autofágica (las llamadas proteínas ATG), la autofagia tiene un importante papel en la protección contra diversas enfermedades, incluyendo el cáncer, las enfermedades inflamatorias o algunos procesos neurodegenerativos. Esta capacidad protectora sugiere que la manipulación de la actividad autofágica podría tener valor terapéutico, una posibilidad que está siendo explorada con intensidad por diversos laboratorios en todo el mundo. Sin embargo, cada vez es más evidente que las diferentes ATGs tienen funciones alternativas no estrictamente relacionadas con la ruta autofágica canónica, bien porque su propósito no es degradativo, o bien porque las ATGs, aún mediando procesos catabólicos, funcionan de formas no convencionales que son fundamentalmente diferentes de la autofagia. La contribución de estas actividades no estrictamente autofágicas a la prevención de las patologías que surgen en ausencia de las ATGs es actualmente desconocida, pero constituye una cuestión de gran interés porque podría determinar la forma en que la función de las ATGs debe ser manipulada con un propósito terapéutico.
Con este objetivo general en mente, en nuestro laboratorio utilizamos la proteína ATG16L1 como paradigma para descubrir y estudiar nuevas actividades no convencionales de la maquinaria autofágica. En su función más canónica, ATG16L1 participa de forma crítica en la formación de los autofagosomas, vesículas citoplasmáticas de doble membrana que secuestran el material que va a ser degradado en el lisosoma a través de la ruta autofágica convencional. Pero ATG16L1 presenta un dominio C-terminal que es irrelevante para esta actividad canónica y parece tener funciones no convencionales en una amplia variedad de procesos celulares. Los proyectos que actualmente se desarrollan en nuestro grupo pretenden identificar y caracterizar con detalle nuevas funciones no canónicas de ATG16L1 y otros miembros de la maquinaria autofágica, y explorar su relación con la ruta convencional. Actividades de interés que estamos estudiando incluyen:
- Regulación la endocitosis, tráfico intracelular y capacidad señalizadora de receptores de membrana
- Control de la estabilidad de mediadores de señalización y su impacto en la regulación de las respuestas inflamatorias
- Regulación de la muerte celular inmunogénica y sus implicaciones en cáncer y en respuesta a la quimioterapia
- Inmunidad innata contra las infecciones bacterianas intracelulares
Para estudiar estos procesos utilizamos una amplia variedad de sistemas experimentales tanto in vitro (líneas celulares) como in vivo (modelos animales) modificados genéticamente mediante el sistema CRISPR/Cas9, así como técnicas proteómicas y aproximaciones bioinformáticas para identificar nuevos mediadores. Actualmente estamos intentando profundizar en estos mecanismos, descubrir nuevos activadores no canónicos de ATG16L1 y evaluar cómo todas estas actividades pueden verse alteradas por un alelo codificante de ATG16L1 (T300A) cuya presencia en homocigosis incrementa el riesgo de sufrir diferentes patologías, incluyendo la enfermedad de Crohn, una grave enfermedad inflamatoria intestinal actualmente incurable. En este contexto, nuestra intención es explorar también las bases moleculares de enfermedades complejas y multifactoriales causadas por el alelo T300A, como la enfermedad de Crohn. Explorar y establecer formas de manipulación de la autofagia atípica con intenciones terapéuticas es un objetivo central del grupo a largo plazo cuyo desarrollo se abordará en los próximos años.
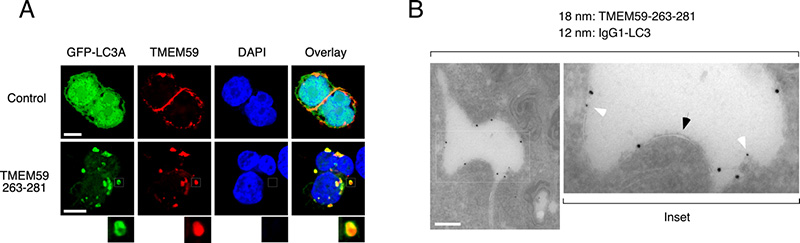
Figura 1. A. Imágenes de microscopía confocal mostrando la identificación de un péptido mínimo en la molécula transmembrana TMEM59 (entre los aminoácidos 269-281) capaz de inducir el marcaje autofágico no convencional de las mismas vesículas endocíticas en las que habita TMEM59. B. Imágenes de microscopía electrónica demostrando que las vesículas marcadas con LC3 presentan una sola membrana, y por tanto son diferentes de los autofagosomas clásicos de doble membrana.
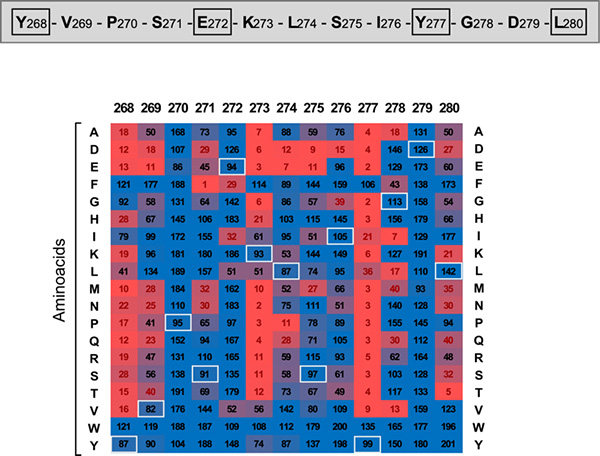
Figura 2. Análisis mutagénico mediante microarrays peptídicos de la unión entre el péptido 269-281 y el dominio WD40 de ATG16L1 con objeto de definir los residuos críticos e identificar un motivo consenso mediador de esta interacción. El péptido nativo se muestra en la parte superior. El heatmap mostrado en la parte inferior incluye valores de unión expresados como el porcentaje de unión al péptido salvaje que es retenido por cada mutante. Los números en negro y rojo indican mutaciones permisivas o prohibitivas respectivamente. Los cuadrados blancos indican los aminoácidos nativos en cada posición. Todas las posiciones están coloreadas siguiendo una escala continua de menos (rojo) a más (azul) actividad de unión.
POSICIONES DISPONIBLES PARA REALIZAR TFG, TFM Y TESIS DOCTORAL: Se ofrecen dos puestos anuales para estudiantes con buen expediente académico, alta motivación e interesados en explorar los mecanismos moleculares que regulan la autofagia no convencional y el papel que estos fenómenos puedan tener en fisiología y patología. Los candidatos interesados deben contactar con el Investigador Principal via email (fxp@cbm.csic.es).

| Apellidos | Nombre | Laboratorio | Ext.* | Categoría profesional | |
|---|---|---|---|---|---|
| Bandera Linero | Julia | 411 | 4738 | julia.bandera(at)cbm.csic.es | Titulado Sup. Actividades Tecn. y Prof.GP1 |
| Oña Sánchez | Daniel | 411 | 4737 | donia(at)cbm.csic.es | M3 66,66% |
| Pimentel Muiños | Felipe X. | 411 | 4737 | fxp(at)cbm.csic.es | E. Investigadores Científicos de Organismos Públicos |
| Terraza Silvestre | Elena | 411 | 4738 | eterraza(at)cbm.csic.es | M3 66,66% |
| Vioque Hacha | Blanca | 411 | 4738 | Estudiante TFM |
Publicaciones relevantes:
- Serramito-Gómez, I; Boada-Romero, E; Villamuera, R; Fernández-Cabrera, A; Cedillo, JL; Martín-Regalado, A; Carding, S; Mayer, U; Powell, PP; Wileman, T; García-Higuera, I; Pimentel-Muiños, FX. (2020). Regulation of cytokine signaling through direct interaction between cytokine receptors and the ATG16L1 WD40 domain. Nat. Commun., 11:5919.
- Serramito-Gómez, S; Boada-Romero, E; Slowicka, K; Vereecke, L; Van Loo, G; Pimentel-Muiños, FX. (2019). The anti-inflammatory protein TNFAIP3/A20 binds the WD40 domain of ATG16L1 to control the autophagic response, NF-kB activation and intestinal homeostasis. Autophagy, 15:1657.
- Slowicka, K; Serramito-Gómez, S; Boada-Romero, E; Martens, A; Sze, M; Petta, I; Vikkula, HK; De Rycke, R; Parthoens, E; Lippens, S; Savvides, SN; Wullaert, A; Vereecke, L; Pimentel-Muiños, FX(*); van Loo, G(*). (2019). Physical and functional interaction between A20 and ATG16L1-WD40 domain in the control of intestinal homeostasis. Nat. Commun., 10:1834. (*) Co-corresponding senior authors
- Gerlach, JP; Jordens, I; Tauriello, DVF; van’t Land-Kuper, I; Bugter, JM; Noordstra, I; van der Kooij, J; Low, TY; Pimentel-Muiños, FX; Xanthakis, D; Fenderico, N; Rabouille, C; Heck, AJR; Egan, DA; Maurice, MM. (2018). TMEM59 potentiates Wnt signaling by promoting signalosome formation. PNAS., 115:E3996.
- Serramito-Gómez, I; Boada-Romero, E; Pimentel-Muiños, FX (2016). Unconventional autophagy mediated by the WD40 domain of ATG16L1 is derailed by the T300A Crohn disease risk polymorphism. Autophagy, 12:2254-2255.
- Boada-Romero, E; Serramito-Gómez, I; Sacristán, MP; Boone, DL; Xavier, RJ; Pimentel-Muiños, FX (2016). The T300A Crohn’s disease risk polymorphism impairs function of the WD40 domain of ATG16L1. Nat. Commun, 7:11821.
- Pimentel-Muiños, FX; Boada-Romero, E. (2014). Selective autophagy against membranous compartments: Canonical and unconventional purposes and mechanisms. Autophagy, 10:397-407.
- Boada-Romero, E; Letek, M; Fleischer, A; Pallauf, K; Ramón-Barros, C; Pimentel-Muiños, FX. (2013). TMEM59 defines a novel ATG16L1-binding motif that promotes local activation of LC3. EMBO J., 32:566-582.
- Rodríguez, DA; Zamorano, S; Lisbona, F; Rojas-Rivera, D; Urra, H; Cubillos-Ruiz, JR; Armisen, R; Henriquez, DR; Cheng, EH; Letek, M; Vaisar, T; Irrazabal, T; Gonzalez-Billault, C; Letai, A; Pimentel-Muiños, FX; Kroemer, G; Hetz, C. (2012). BH3-only proteins are part of a regulatory network that controls the sustained signaling of the unfolded protein response sensor IRE1a. EMBO J., 31:2322-2335.
- Klee, M; Pallauf, K; Alcalá, S; Fleischer, A; Pimentel-Muiños, FX. (2009). Mitochondrial apoptosis induced by BH3-only molecules in the exclusive presence of endoplasmic reticular Bak. EMBO J., 28:1757-1768




















