Bases moleculares de la plasticidad neuronal
Resumen de Investigación:
Los recuerdos están codificados por cambios a largo plazo en la eficiencia sináptica y la conectividad. Un conocimiento profundo de las bases moleculares de la regulación de la comunicación sináptica es fundamental para descifrar los mecanismos involucrados en la formación de los recuerdos. Nuestro grupo estudia los mecanismos celulares y moleculares que modulan la plasticidad de las redes neuronales, con el objetivo de encontrar dianas moleculares y estrategias efectivas que contribuyan a mejorar el rendimiento cognitivo. La actividad sináptica desencadena oscilaciones intracelulares de calcio (Ca+2) que modulan localmente distintas vías de señalización. Calmodulina (CaM), una proteína que une calcio, traduce estas oscilaciones en eventos de señalización intracelular. La disponibilidad y actividad de CaM están reguladas localmente por proteínas como Neurogranina (Ng), muy abundante en el entorno postsináptico. Ng secuestra CaM de manera dependiente de Ca+2 y fosforilación. En nuestro laboratorio, utilizamos varias preparaciones que incluyen cultivos primarios de neuronas disociadas para comprender el papel de Ng en los mecanismos subyacentes a la plasticidad sináptica, como los asociados a plasticidad hebbiana (potenciación a largo plazo -LTP- y depresión a largo plazo -LTD) y a plasticidad homeostática (escalado sináptico). Para ello utilizamos una combinación de técnicas de bioquímica, biología molecular, electrofisiología, microscopía avanzada y otras técnicas de imagen. Dado que los niveles de Ng y el rendimiento cognitivo se encuentran estrechamente correlacionados, estamos interesados en comprender los mecanismos que regulan la transcripción de Ng y su traducción local en las dendritas. Proponemos Ng como diana molecular para diseñar estrategias orientadas a prevenir, tratar o aliviar condiciones y patologías asociadas a una función cognitiva deteriorada. Justificamos este objetivo sobre las siguientes premisas. Primero, la expresión de Ng tiene lugar de forma casi exclusiva en el cerebro. Su deficiencia en ratones no causa anormalidades anatómicas o fisiológicas aparentes, pero sí alteraciones cognitivas graves. Y en segundo lugar, utilizar Ng como diana para mejorar la función cognitiva muy probablemente carezca de efectos secundarios importantes, ya que su expresión está muy regulada espacio-temporalmente (Ng solamente se expresa en prosencéfalo postnatal) y específicamente asociada al rendimiento cognitivo. Una comprensión más amplia y profunda del papel que juegan Ng y otras proteínas que secuestran CaM en los mecanismos de plasticidad neuronal contribuirá al desarrollo de nuevas terapias para mejorar la función cognitiva y la calidad de vida de personas mayores y pacientes que sufren de enfermedades neurológicas.
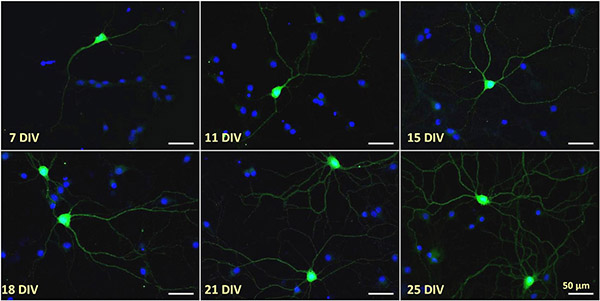
Figura 1.
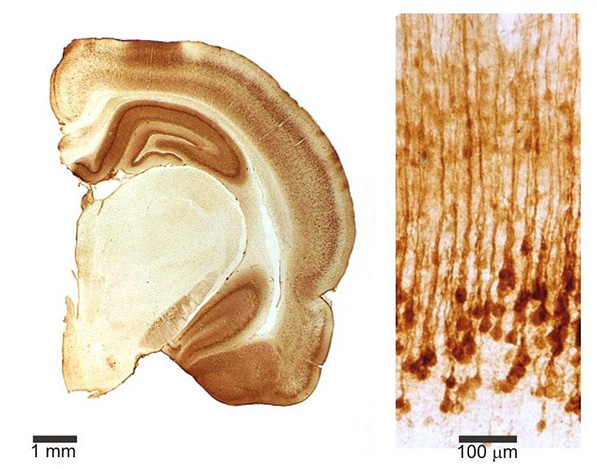
Figura 2.
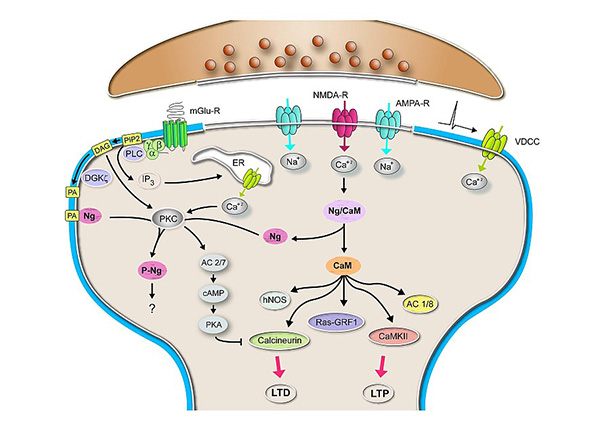
Figura 3.

| Apellidos | Nombre | Laboratorio | Ext.* | Categoría profesional | |
|---|---|---|---|---|---|
| Anushka Dogra | Kiran | 307 | 4612 | Estudiante | |
| Cadenato Martínez de Salinas | Pedro | 307 | 4612 | Estudiante TFM | |
| Díez Guerra | Fco. Javier | 307 | 4612 | fjdiez(at)cbm.csic.es | Catedrático Universidad, GA |
| Martínez Blanco | Elena | 307 | 4642 | elena.martinez(at)cbm.csic.es | Investigador |
Publicaciones relevantes:
- Alberto Garrido-García, Raquel de Andrés, Amanda Jiménez-Pompa, Patricia Soriano, Diego Sanz-Fuentes, Elena Martínez-Blanco, F Javier Díez-Guerra. “Neurogranin Expression Is Regulated by Synaptic Activity and Promotes Synaptogenesis in Cultured Hippocampal Neurons”. Molecular Neurobiology 56 (11), 7321-7337 (Nov 2019). DOI: 10.1007/s12035-019-1593-3. PMID 31020616.
- Dolores Piniella, Elena Martínez-Blanco, Ignacio Ibáñez, David Bartolomé-Martín, Eva Porlán, F Javier Díez-Guerra, Cecilio Giménez, Francisco Zafra. “Identification of Novel Regulatory Partners of the Glutamate Transporter GLT-1”. Glia 66 (12), 2737-2755 (Dec 2018). DOI: 10.1002/glia.23524. PMID: 30394597
- Marta Pérez-Hernández, Marcos Matamoros, Silvia Alfayate, Paloma Nieto-Marín, Raquel G Utrilla, David Tinaquero, Raquel de Andrés, Teresa Crespo, Daniela Ponce-Balbuena, B Cicero Willis, Eric N Jiménez-Vázquez, Guadalupe Guerrero-Serna, André M da Rocha, Katherine Campbell, Todd J Herron, F Javier Díez-Guerra, Juan Tamargo, José Jalife, Ricardo Caballero, Eva Delpón. “Brugada Syndrome Trafficking-Defective Nav1.5 Channels Can Trap Cardiac Kir2.1/2.2 Channels”. Journal of Clinical Investigation Insight 2018;3(18):e96291. DOI: 10.1172/jci.insight.96291. PMID: 30232268.
- Daniela Ponce-Balbuena, Guadalupe Guerrero-Serna, Carmen R Valdivia, Ricardo Caballero, F Javier Diez-Guerra, Eric N Jiménez-Vázquez, Rafael J Ramírez, André Monteiro da Rocha, Todd J Herron, Katherine F Campbell, B Cicero Willis, Francisco J Alvarado, Manuel Zarzoso, Kuljeet Kaur, Marta Pérez-Hernández, Marcos Matamoros, Héctor H Valdivia, Eva Delpón, José Jalife. “Cardiac Kir2.1 and Na V 1.5 Channels Traffic Together to the Sarcolemma to Control Excitability”. Circulation Research 122(11):1501-1516 (May 2018). DOI: 10.1161/CIRCRESAHA.117.311872. PMID: 29514831.
- Raquel G Utrilla, Paloma Nieto-Marín, Silvia Alfayate, David Tinaquero, Marcos Matamoros, Marta Pérez-Hernández, Sandra Sacristán, Lorena Ondo, Raquel de Andrés, F Javier Díez-Guerra, Juan Tamargo, Eva Delpón, Ricardo Caballero. “Kir2.1-Nav1.5 Channel Complexes Are Differently Regulated Than Kir2.1 and Nav1.5 Channels Alone”. Frontiers in Physiology 8, 903 (Nov 2017). DOI: 10.3389/fphys.2017.00903. PMID: 29184507.
- Ignacio Ibáñez, F Javier Díez-Guerra, Cecilio Giménez, Francisco Zafra. “Activity Dependent Internalization of the Glutamate Transporter GLT-1 Mediated by β-Arrestin 1 and Ubiquitination”. Neuropharmacology 107, 376-386 (Aug 2016). DOI: 10.1016/j.neuropharm.2016.03.042. PMID: 27044663.
- José P Ferraz-Nogueira, F Javier Díez-Guerra, Juan Llopis. “Visualization of Phosphatidic Acid Fluctuations in the Plasma Membrane of Living Cells”. PLos One 9 (7), e102526 (Jul 2014). DOI: 10.1371/journal.pone.0102526. PMID: 25025521.
- Ana Quintas, Alain J de Solís, F Javier Díez-Guerra, José M Carrascosa, Elena Bogónez. “Age-associated Decrease of SIRT1 Expression in Rat Hippocampus: Prevention by Late Onset Caloric Restriction”. Experimental Gerontology 47 (2), 198-201 (Feb 2012). DOI: 10.1016/j.exger.2011.11.010. PMID: 22143179.
- Carlos Sánchez, Mª Ángeles Muñoz, Maite Villalba, Verónica Labrador, F Javier Díez-Guerra. “Setting Up and Running an Advanced Light Microscopy and Imaging Facility”. Current Protocols Cytometry Chapter 12, Unit 12.22 (Jul 2011). DOI: 10.1002/0471142956.cy1222s57. PMID: 21732308.
- F Javier Díez-Guerra. “Neurogranin, a link between calcium/calmodulin and protein kinase C signaling in synaptic plasticity”. IUBMB Life 62(8):597-606 (2010). DOI: 10.1002/iub.357. PMID: 20665622.
- Alberto Garrido-García, Beatriz Andrés-Pans, Lara Durán-Trío, F Javier Díez-Guerra. “Activity-dependent Translocation of Neurogranin to Neuronal Nuclei”. Biochemical Journal 424 (3), 419-29 (Dec 2009). DOI: 10.1042/BJ20091071. PMID: 19751214.
- Irene Domínguez-González, Silvia N Vázquez-Cuesta, Alicia Algaba, F Javier Díez-Guerra. “Neurogranin Binds to Phosphatidic Acid and Associates to Cellular Membranes”. Biochemical Journal 404 (1), 31-43 (May 2007). DOI: 10.1042/BJ20061483. PMID: 17295609.
- Enrique Fernández-Sánchez, F Javier Díez-Guerra, Beatriz Cubelos, Cecilio Giménez, Francisco Zafra. “Mechanisms of Endoplasmic-Reticulum Export of Glycine transporter-1 (GLYT1)”. Biochemical Journal 409 (3), 669-81 (Feb 2008). DOI: 10.1042/BJ20070533. PMID: 17919119.




















