Inflamación vascular y autofagia
Resumen de Investigación:
La inflamación está en la base de una plétora de enfermedades con orígenes etiológicos muy diferentes. Aunque esta reacción inmunitaria desempeña un papel primordial durante la supervivencia del huésped y la reparación de los tejidos, la inflamación debe estar estrictamente regulada para evitar un daño excesivo de los tejidos y la instigación de enfermedades inflamatorias. Por ejemplo, la infiltración descontrolada de células inmunitarias desde los vasos sanguíneos a los tejidos lesionados, así como una permeabilidad vascular aberrante, pueden conducir al desarrollo de numerosas patologías, entre ellas afecciones cardiovasculares, metabólicas e infecciosas de gran prevalencia, así como la progresión tumoral. Por lo tanto, comprender los mecanismos por los que la vasculatura se vuelve disfuncional durante la inflamación patológica es un área de investigación de enorme interés.
En los últimos años se ha descrito que la autofagia, un proceso metabólico, de control de la calidad del citoplasma y homeostático en general, es también clave para la correcta función del sistema inmunitario. Hasta ahora, la mayoría de esta evidencia proviene de la regulación por parte de la autofagia de la supervivencia, diferenciación, polarización y generación de mediadores inflamatorios de las propias células inmunitarias. Sin embargo, recientemente nuestro grupo ha demostrado que los procesos de autofagia de las células endoteliales, el portal que gobierna la entrada de leucocitos y macromoléculas a los tejidos, son esenciales para limitar el reclutamiento tisular de neutrófilos durante la inflamación aguda, así como el daño tisular asociado (Reglero-Real et al. Immunity, 2021). A pesar de ello, aún se desconocen los mecanismos moleculares y la naturaleza de los procesos de autofagia que regulan este fenómeno. Por lo tanto, el principal objetivo de nuestro laboratorio emergente es descifrar los mecanismos moleculares a través de los cuales las vías de autofagia endotelial configuran la respuesta inflamatoria con el fin de identificar nuevas dianas terapéuticas para el tratamiento de enfermedades con un componente inflamatorio. En conjunto, pretendemos explorar los factores iniciadores, las características moleculares y la relevancia fisiopatológica de los procesos de autofagia endotelial durante la inflamación aguda y crónica.
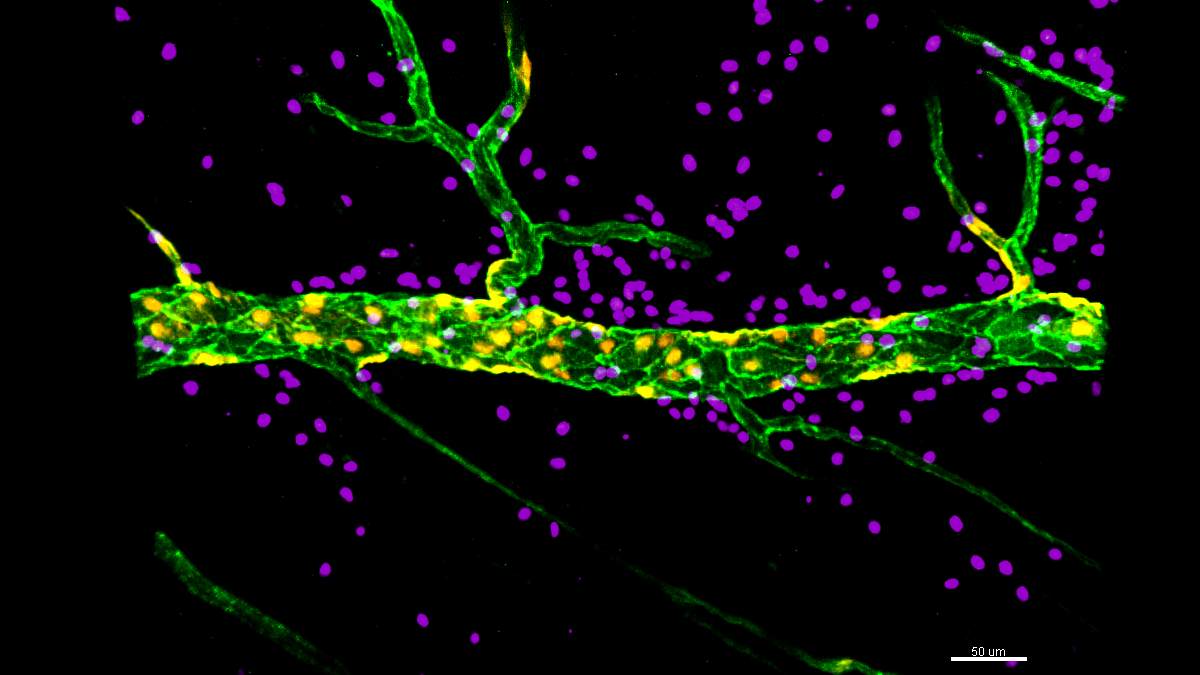
Figura 1. Imágenes confocales de vénulas postcapilares inflamadas del músculo cremáster marcadas para las uniones endoteliales (PECAM-1; verde) y neutrófilos (MRP14; morado).
Vídeo 1. Vídeo de microscopía confocal intravital de vénulas postcapilares inflamadas del músculo cremáster de ratones con células endoteliales Wild Type (WT; blanco) o deficientes en autofagia (Atg5-/-; magenta). El vídeo sigue la migración de 4 neutrófilos luminales (verde) a través de la misma unión Atg5-/- e ilustra que las uniones deficientes en autofagia tienen una gran capacidad para sostener la migración transendotelial de neutrófilos. Cada evento individual de migración de neutrófilos se asocia con la formación transitoria de un poro entre las uniones endoteliales marcadas con anti- PECAM-1.

| Apellidos | Nombre | Laboratorio | Ext.* | Categoría profesional | |
|---|---|---|---|---|---|
| Reglero Real | Natalia | 320 | 4652 | nreglero[at]cbm.csic.es | Investigadora Ramón y Cajal |
| García Mateos | Dafne | 320 | 4652 | dafne.garcia[at]cbm.csic.es | Técnico Superior UAM |
| Armesto | Edurne | 320 | 4652 | Estudiante TFG |
Publicaciones relevantes:
- Endothelial cell autophagy keeps neutrophil trafficking under control. Reglero-Real N*, Pérez-Gutiérrez L and Sussan Nourshargh. (2021). Autophagy Oct 31:1-3. (* corresponding author) doi: 10.1080/15548627.2021.1987675.
- Autophagy modulates endothelial junctions to restrain neutrophil diapedesis during inflammation. Reglero-Real N†*, Pérez-Gutiérrez L†, Yoshimura A, Rolas L, Garrido-Mesa J, Barkaway A, Pickworth C, Saleeb RS, Gonzalez-Nuñez M, Austin-Williams SN, Cooper D, Vázquez-Martínez L, Fu T, De Rossi G, Golding M, Benoit-Voisin M, Boulanger CM, Kubota Y, Muller WA, Tooze SA, Nightingale TD, Collinson L, Perretti M, Aksoy E and Nourshargh S*. (2021). Immunity Sep 14;54(9):1989-2004. (†co-first author; *co-corresponding author). doi: 10.1016/j.immuni.2021.07.012.
- Age-related cellular and molecular changes in the local inflammatory milieu cause aberrant neutrophil trafficking in vivo. Barkaway A, Rolas L, Joulia R, Bodkin J, Lenn T, Owen-Woods C, Reglero-Real N, Stein M, Vázquez-Martínez L, Girbl T, Poston RN, Golding M, Saleeb RS, Thiriot A, von Andrian UH, Duchene J, Voisin MB, Bishop CL, Voehringer D, Roers A, Rot A, Lämmermann T, Nourshargh S. (2021) Immunity Jul 13;54(7):1494-1510. doi: 10.1016/j.immuni.2021.04.025.
- Time to Take Time Seriously. Reglero-Real N†*, Rolas L†*, Nourshargh S*. (2019) Leukocyte Trafficking: Immunity Feb 19;50(2); 273-275. (†co-first author; *co-corresponding author) doi: 10.1016/j.immuni.2019.01.013.
- Endothelial cell junctional adhesion molecules: Role and Regulation of Expression in inflammation. Reglero-Real N†, Colom B†, Bodkin JV, Nourshargh S. (2016). Arteriosclerosis, Thrombosis and Vascular Biology Oct;36(10); 2048-2057. (†co-first author) # Cover Image of the 2016 Oct. Issue. doi: 10.1161/ATVBAHA.116.307610.
- Cellular Barriers after Extravasation: Leukocyte Interactions with Polarized Epithelia in the Inflamed Tissue. Reglero-Real N, García-Weber D, Millán J. (2016) Mediators of Inflammation 2016; 7650260. doi: 10.1155/2016/7650260.
- Apicobasal polarity controls lymphocyte adhesion to hepatic epithelial cells. Reglero-Real N, Alvarez-Varela A, Cernuda-Morollón E, Feito J, Marcos-Ramiro B, Fernández-Martín L, Gómez-Lechón MJ, Muntane J, Sandoval P, Majano PL, Correas I, Alonso MA and Millán J. (2014) Cell Reports Sep 25;8(6); 1879-1893. doi: 10.1016/j.celrep.2014.08.007.
- Endothelial membrane reorganization during leukocyte extravasation. Reglero-Real N, Marcos-Ramiro B, Millan J. (2012). Cellular and Molecular Life Sciences, Sep;69-18; 3079-3099. doi: 10.1007/s00018-012-0987-4.




















